ГДЗ Химия 8 класс Габриелян, Остроумов, Сладков на Решалка
- Учебники
- 8 класс
- Химия 👍
- Габриелян
ГДЗ Химия 8 класс Габриелян, Остроумов, Сладков
авторы: Габриелян, Остроумов, Сладков.
издательство: «Просвещение»
Задачи
- ГЛАВА I. Первоначальные химические понятия
- §1. Предмет химии. Роль химии в жизни человека
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.6)
- ?
- Лабораторный опыт 1
- 1
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- Используйте дополнительную информацию
- 7
- 8
- 9
- 10
- Вопрос в начале параграфа
- §2.
 Методы изучения химии
Методы изучения химии- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- Используйте дополнительную информацию
- 6
- 7
- Вопрос в начале параграфа
- §3. Агрегатные состояния веществ
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 2
- 1
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- Используйте дополнительную информацию
- 5
- 6
- Вопрос в начале параграфа
- Практическая работа 1
- Вопрос в начале работы
- ✓
- Вопрос в начале работы
- Практическая работа 2
- Вопрос в начале работы
- ✓
- Опыт 1. Физические явления при горении свечи
- 1
- Опыт 2.
 Строение пламени свечи
Строение пламени свечи- 1
- Опыт 3. Обнаружение продуктов горения парафина и влияние воздуха на горение свечи
- 1
- Дополнительное задание
- 1
- Вопрос в начале работы
- §4. Физические явления — основа разделения смесей в химии
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 3
- 1
- Лабораторный опыт 4
- 1
- Вопрос (стр.26)
- ?
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- Используйте дополнительную информацию
- 5
- 6
- Вопрос в начале параграфа
- Практическая работа 3
- Вопрос в начале работы
- ✓
- Опыт 1. Механический анализ почвы
- 1
- Опыт 2. Получение почвенного раствора и опыты с ним
- 1
- Дополнительное задание
- «>.
- Вопрос в начале работы
- §1. Предмет химии. Роль химии в жизни человека
- §5. Атомно-молекулярное учение. Химические элементы
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.31)
- ?
- Вопрос (стр.32)
- ?
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- Используйте дополнительную информацию
- 7
- 8
- Вопрос в начале параграфа
- §6. Знаки химических элементов. Переодическая таблица Д.И.Менделеева
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.37)
- ?
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- 8
- Используйте дополнительную информацию
- 9
- Вопрос в начале параграфа
- §7.
 Химические формулы
Химические формулы- Вопрос в начале параграфа
- ✓
- Вопрос (стр.40)
- ?
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Используйте дополнительную информацию
- 11
- Вопрос в начале параграфа
- §8. Валентность
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- Примените свои знания
- 6
- 7
- Используйте дополнительную информацию
- 8
- 9
- Вопрос в начале параграфа
- §9. Химические реакции
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 5
- 1
- Лабораторный опыт 6
- 1
- Лабораторный опыт 7
- 1
- Вопрос (стр.
 47)
47)- ?
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- 7
- Используйте дополнительную информацию
- 8
- 9
- Вопрос в начале параграфа
- §10. Химические уравнения
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 8
- 1
- Лабораторный опыт 9
- 1
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- 8
- Используйте дополнительную информацию
- 9
- Вопрос в начале параграфа
- §11. Типы химических реакций
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 10
- 1
- Лабораторный опыт 11
- 1
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Используйте дополнительную информацию
- 11
- Вопрос в начале параграфа
 Важнейшие представители неорганических веществ. Количественные отношения в химии
Важнейшие представители неорганических веществ. Количественные отношения в химии- §12. Воздух и его состав
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- Примените свои знания
- 8
- Используйте дополнительную информацию
- 9
- Вопрос в начале параграфа
- §13. Кислород
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- Примените свои знания
- 6
- 7
- Используйте дополнительную информацию
- 8
- 9
- Вопрос в начале параграфа
- Практическая работа 4
- Вариант 1
- 1
- Вариант 2
- 1
- Вариант 1
- §14.
 Оксиды
Оксиды- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 12
- 1
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- Используйте дополнительную информацию
- 6
- Вопрос в начале параграфа
- §15. Водород
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 13
- 1
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- Используйте дополнительную информацию
- 6
- 7
- Вопрос в начале параграфа
- Практическая работа 5
- 5
- §16. Кислоты
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 14
- 1
- Вопрос (стр.
 76)
76)- ?
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- Используйте дополнительную информацию
- 5
- 6
- Вопрос в начале параграфа
- §17. Соли
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- Используйте дополнительную информацию
- 7
- 8
- Вопрос в начале параграфа
- §18. Количество вещества
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- Используйте дополнительную информацию
- 8
- Вопрос в начале параграфа
- §19.
 Молярный объем газов
Молярный объем газов- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Используйте дополнительную информацию
- 11
- Вопрос в начале параграфа
- §20. Расчеты по химическим уравнениям
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- Используйте дополнительную информацию
- 5
- 6
- 7
- Вопрос в начале параграфа
- §21. Вода. Основания
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.90)
- ?
- Лабораторный опыт 15
- 1
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- Используйте дополнительную информацию
- 7
- Вопрос в начале параграфа
- §22.
 Растворы. Массовая доля растворенного вещества
Растворы. Массовая доля растворенного вещества- Лабораторный опыт 16
- 1
- Вопрос (стр.93)
- ?
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Используйте дополнительную информацию
- 11
- Лабораторный опыт 16
- Практическая работа 6
- Вопрос в начале работы
- ✓
- Вариант 1
- 1
- 2
- 3
- Вариант 2
- 1
- 2
- 3
- Вариант 3
- 1
- 2
- 3
- Вариант 4
- 1
- 2
- 3
- Вопрос в начале работы
- Домашний эксперимент
- Вопрос в начале эксперемента
- ✓
- Отчет о проделанной работе
- 1
- Вопрос в начале эксперемента
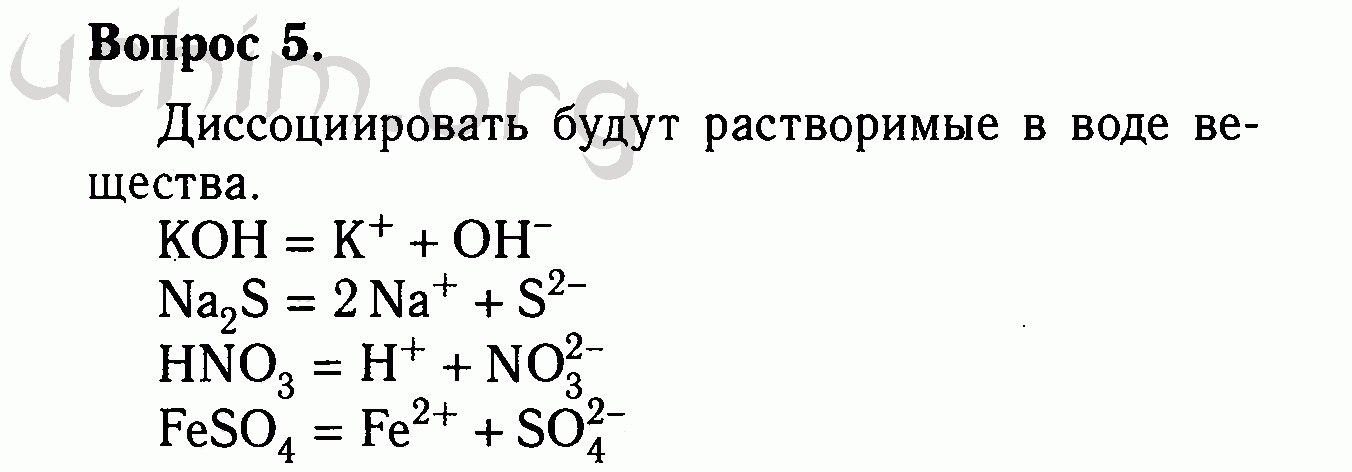 Основные классы неорганических соединений
Основные классы неорганических соединений- §23. Оксиды, их классификация и химические свойства
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 17
- 1
- Вопрос (стр.102)
- ?
- Вопрос (стр.103)
- ?
- Лабораторный опыт 18
- 1
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- Используйте дополнительную информацию
- 7
- Вопрос в начале параграфа
- §24. Основания, их классификация и химические свойства
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 19
- 1
- Лабораторный опыт 20
- 1
- Лабораторный опыт 21
- 1
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- Используйте дополнительную информацию
- 7
- Вопрос в начале параграфа
- §25.
 Кислоты, их классификация и химические свойства
Кислоты, их классификация и химические свойства- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 22
- 1
- Лабораторный опыт 23
- 1
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- Примените свои знания
- 6
- 7
- 8
- 9
- 10
- 11
- Используйте дополнительную информацию
- 12
- Вопрос в начале параграфа
- §26. Соли, их классификация и химические свойства
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 24
- 1
- Лабораторный опыт 25
- 1
- Лабораторный опыт 26
- 1
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- 7
- Используйте дополнительную информацию
- 8
- Вопрос в начале параграфа
- §27.
 Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений- Вопрос в начале параграфа
- ✓
- Вопрос (стр.118)
- ?
- Лабораторный опыт 27
- 1
- Проверьте свои знания
- 1
- Примените свои знания
- 2
- 3
- 4
- 5
- 6
- 7
- Используйте дополнительную информацию
- 8
- Вопрос в начале параграфа
- Практическая работа 7
- Вопрос в начале работы
- ✓
- Реакция нейтрализации
- 1
- Получение соединений
- 2
- Идентификация кислоты
- 3
- Идентификация основания
- 4
- Идентификация солей
- 5
- Вопрос в начале работы
 И.Менделеева. Строение атома
И.Менделеева. Строение атома- §28. Естественные семейства химических элементов. Амфотерность
- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 28
- 1
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- Примените свои знания
- 6
- 7
- 8
- 9
- Выразите свое мнение
- 10
- Вопрос в начале параграфа
- §29. Открытие периодического закона Д.И.Менделеева
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- Используйте дополнительную информацию
- 7
- 8
- Вопрос в начале параграфа
- §30. Основные сведения о строении атома
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- 7
- 8
- Используйте дополнительную информацию
- 9
- Вопрос в начале параграфа
- §31.
 Строение электронных оболочек атомов
Строение электронных оболочек атомов- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- Используйте дополнительную информацию
- 12
- Вопрос в начале параграфа
- §32. Периодическая система химических элементов Д.И.Менделеева
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.141)
- ?
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- Выразите свое мнение
- 7
- Вопрос в начале параграфа
- §33. Характеристика элемента по его положению в периодической системе
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- 5
- 6
- Примените свои знания
- 7
- 8
- 9
- 10
- 11
- Используйте дополнительную информацию
- 12
- Вопрос в начале параграфа
 Химическая связь. Окислительно-восстановительные реакции
Химическая связь. Окислительно-восстановительные реакции- §34. Ионная химическая связь
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- Используйте дополнительную информацию
- 6
- Вопрос в начале параграфа
- §35. Ковалентная химическая связь
- Вопрос в начале параграфа
- ✓
- Вопрос (стр.154)
- ?
- Проверьте свои знания
- 1
- 2
- 3
- Примените свои знания
- 4
- 5
- 6
- Выразите свое мнение
- 7
- Вопрос в начале параграфа
- §36. Ковалентная неполярная и полярная химическая связь
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- Используйте дополнительную информацию
- 7
- Вопрос в начале параграфа
- §37.
 Металлическая химическая связь
Металлическая химическая связь- Вопрос в начале параграфа
- ✓
- Лабораторный опыт 29
- 1
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- 7
- Используйте дополнительную информацию
- 8
- Вопрос в начале параграфа
- §38. Степень окисления
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- Примените свои знания
- 3
- 4
- 5
- 6
- Используйте дополнительную информацию
- 7
- Вопрос в начале параграфа
- §39. Окислительно-восстановительные реакции
- Вопрос в начале параграфа
- ✓
- Проверьте свои знания
- 1
- 2
- 3
- 4
- Примените свои знания
- 5
- 6
- 7
- 8
- 9
- Используйте дополнительную информацию
- 10
- Вопрос в начале параграфа
ВПР по химии 8 класс 2021 Варианты с ответами
В период с 15 марта по 21 мая 2021 года в очередной раз состоялись всероссийские проверочные работы по химии в 8 классах.
После проведения ВПР в школах стали доступны реальные варианты и критерии оценки.
Для каждой школы варианты формировались индивидуально из банка заданий ВПР.
→ купить рабочие тетради ВПР по химии для 8 класса
ВПР 2021 по химии для 8 класса с ответами
Структура проверочной работы ВПР 2021 по химии 8 класс
Вариант проверочной работы состоит из 9 заданий, которые различаются по содержанию и проверяемым требованиям.
Задания 1, 2, 7.3 основаны на изображениях конкретных объектов и процессов, требуют анализа этих изображений и применения химических знаний при решении практических задач.
Задание 5 построено на основе справочной информации и предполагает анализ реальной жизненной ситуации.
Задания 1, 3.1, 4, 6.2, 6.3, 8 и 9 требуют краткого ответа.
Остальные задания проверочной работы предполагают развернутый ответ.
КИМ ВПР 8 класса направлены на проверку у обучающихся предметных требований:
1) формирование первоначальных систематизированных представлений о веществах, их превращениях и практическом применении; овладение понятийным аппаратом и символическим языком химии;
2) осознание объективной значимости основ химической науки как области современного естествознания, химических превращений неорганических и органических веществ как основы многих явлений живой и неживой природы; углубление представлений о материальном единстве мира;
3) овладение основами химической грамотности: способностью анализировать и объективно оценивать жизненные ситуации, связанные с химией, навыками безопасного обращения с веществами, используемыми в повседневной жизни; умением анализировать и планировать экологически безопасное поведение в целях сохранения здоровья и окружающей среды;
4) формирование умений устанавливать связи между реально наблюдаемыми химическими явлениями и процессами, происходящими в микромире, объяснять причины многообразия веществ, зависимость их свойств от состава и строения, а также зависимость применения веществ от их свойств;
5) приобретение опыта использования различных методов изучения веществ: наблюдения за их превращениями при проведении несложных химических экспериментов с использованием лабораторного оборудования и приборов;
6) формирование представлений о значении химической науки в решении современных экологических проблем, в том числе в предотвращении техногенных и экологических катастроф.
Тексты заданий в КИМ ВПР 8 класса в целом соответствуют формулировкам, принятым в учебниках, включенных в Федеральный перечень учебников, допущенных к использованию при реализации имеющих государственную аккредитацию образовательных программ основного общего образования
Связанные страницы:
Демоверсия ВПР 2021 по химии 8 класс
Подготовка к ВПР по химии в 8 классе
Подготовка к ВПР по химии в 11 классе
Демоверсия ВПР 2021 по биологии 8 класс
CHEMISTRY-TEXT 8th Edition Textbook Solutions
Skip to main content
Literature guidesConcept explainersWriting guidePopular textbooksPopular high school textbooksPopular Q&ABusinessAccountingEconomicsFinanceLeadershipManagementMarketingOperations ManagementEngineeringBioengineeringChemical EngineeringCivil EngineeringComputer EngineeringComputer ScienceElectrical EngineeringMechanical EngineeringLanguageSpanishMathAdvanced MathAlgebraCalculusGeometryProbabilityStatisticsTrigonometryScienceAdvanced PhysicsAnatomy and PhysiologyBiochemistryBiologyChemistryEarth ScienceHealth & NutritionNursingPhysicsSocial ScienceAnthropologyGeographyHistoryPolitical SciencePsychologySociology
learn
write
plus
Log In
Sign Up
ScienceChemistryCHEMISTRY-TEXT
Buy this textbookBuy launch
CHEMISTRY-TEXT
8th Edition
Robinson
Publisher: PEARSON
ISBN: 9780134856230
Глава
1. Химические инструменты. Эксперименты и измерения. Структуры8 Ковалентные соединения Теории связи и молекулярная структура9Термохимия Химическая энергия10 Газы, их свойства и поведение11 Жидкости и фазовые превращения12 Твердые тела и твердотельные материалы13 Растворы и их свойства14 Химическая кинетика15 Химическое равновесие16 Водные равновесия: кислоты и основания17 Применение водных равновесий18 Термодинамика: энтропия, свободная энергия и спонтанность19 Электрохимия20 Ядерная химия21 Переходные элементы И координационная химия22 Элементы основной группы23 Органическая и биологическая химия
Химические инструменты. Эксперименты и измерения. Структуры8 Ковалентные соединения Теории связи и молекулярная структура9Термохимия Химическая энергия10 Газы, их свойства и поведение11 Жидкости и фазовые превращения12 Твердые тела и твердотельные материалы13 Растворы и их свойства14 Химическая кинетика15 Химическое равновесие16 Водные равновесия: кислоты и основания17 Применение водных равновесий18 Термодинамика: энтропия, свободная энергия и спонтанность19 Электрохимия20 Ядерная химия21 Переходные элементы И координационная химия22 Элементы основной группы23 Органическая и биологическая химия
Раздел
Вопросы главы
Задача 1.1P:
Выразите диаметр наночастицы (0,000 000 050 м) в экспоненциальной записи, а затем выразите…
Задача 1.2A:
ПРИМЕНИТЬ научное обозначение с использованием основных единиц СИ массы…
Задача 1.3P:
ПРАКТИКА 1.3 Температура плавления поваренной соли 1474oF. Какая это температура по Цельсию и…
Какая это температура по Цельсию и…
Задача 1.4A
Задача 1.5P
Задача 1.6A
Задача 1.7P
Задача 1.8A
Задача 1.9P:
Сколько значащих цифр имеет каждая из следующих величин? (a) 0,003 00 мл(b) 2070…
Задача 1.10A:
Прочитайте объем бюретки и запишите свой ответ с правильным количеством значащих цифр.
Задача 1.11P
Задача 1.12A:
Образец ацетона объемом 1,000 мл, обычного растворителя, используемого для удаления краски, был помещен в небольшой флакон…
Задача 1.13P:
Выполните следующие вычисления, выражая каждый результат правильным числом значащих… максимальные размеры футбольного поля составляют 90,0 м в ширину и 120,0 м в длину, что дает площадь…0004 Problem 1.23P
Problem 1.24P
Problem 1.25P
Problem 1.26P
Problem 1.27CP
Problem 1.28CP
Problem 1.29CP
Problem 1.30CP
Problem 1.31CP
Problem 1. 32SP
32SP
Задача 1.33SP
Задача 1.34SP
Задача 1.35SP
Задача 1.36SP
Проблема 1.37SP
Проблема 1.38SP
Задача 1.39SP:
Префиксы для множества подразделений SI используются для выражения крупных и малых префиксов для множества подразделений SI. количества. Завершить…
Задача 1.40SP
Задача 1.41SP
Проблема 1.42SP
Проблема 1.43SP
Проблема 1.44SP
Проблема 1.45SP
Проблема 1.46SP
Проблема 1.47SP
Проблема 1.48SP
4SP.
Задача 1.50SP
Задача 1.51SP
Задача 1.52SP
Задача 1.53SP
Проблема 1.54SP
Проблема 1.55SP
Проблема 1.56SP
Проблема 1.57SP: 9000SP.0003
Вольфрам, элемент, используемый для изготовления нитей накаливания в лампочках, имеет температуру плавления 6192 °F. Конвертировать…
Задача 1.58SP:
Предположим, вас не устраивают единицы Цельсия и Фаренгейта и вы хотите создать свою собственную. .. мл пробы воды при 293,2 К нагревали в течение 8 мм 25 с до получения постоянной температуры…
.. мл пробы воды при 293,2 К нагревали в течение 8 мм 25 с до получения постоянной температуры…
Задача 1.62СП
Задача 1.63СП
Задача 1.64SP
Задача 1.65SP
Проблема 1.66SP
Проблема 1.67SP
Проблема 1.68SP
Проблема 1.69SP
Проблема 1.70SP
Проблема 1.71SP
Проблема 1.72sp
40004.
Проблема 1.74SP
Задача 1.75SP
Задача 1.76SP
Задача 1.77SP
Проблема 1.78SP
Проблема 1.79SP
Проблема 1.80SP
Проблема 1.81SP
Проблема 1.82SP
Задача 1.83SP
Проблема 1.84SP
Задача 1.85SP
Проблема 1.86SP
Проблема 1.87SP
Проблема 1.88SP
Проблема 1.89SP
Проблема 1.90SP
40004 40004.
Задача 1.92SP
Задача 1.93SP
Задача 1.94SP
Задача 1.95SP
Проблема 1.96SP
Проблема 1.97SP
Проблема 1.98SP
Проблема 1. 99SP
99SP
Задача 1.100SP
Задача 1.101SP
Проблема 1.102SP
Задача 1.103SP
Проблема 1.104SP
Проблема 1.105SP
Проблема 1.106SP
Проблема 1.107MP
. Проблема 1.108MP
1,107MP
1.108MP
49.101MP.
Задача 1.110 Мр
Задача 1.111MP
Задача 1.112MP
Задача 1.113MP
Проблема 1.114MP
Задача 1.115MP
Проблема 1.116 М.П.:
.0004 Калибровочную колбу до метки 25,00 мл наполнили этиловым спиртом. Взвешивая колбу перед…
Задача 1.117MP:
Латунь представляет собой медно-цинковый сплав. Какова масса в граммах латунного цилиндра длиной 1,62…
Задача 1.118MP
Задача 1.119MP:
Элемент галлий (Ga) имеет второй по величине диапазон жидкого состояния среди всех элементов, плавясь при 29,78° C и…
Ключ к ответу Глава 8 — Химия
1.
Сходства: Оба типа связей возникают в результате перекрытия атомных орбиталей соседних атомов и содержат максимум два электрона. Различия: σ-связи прочнее и являются результатом сквозного перекрытия, а все одинарные связи являются σ-связями; π-связи между одними и теми же двумя атомами слабее, потому что они возникают в результате параллельного перекрытия, а множественные связи содержат одну или несколько π-связей (в дополнение к σ-связи).
Различия: σ-связи прочнее и являются результатом сквозного перекрытия, а все одинарные связи являются σ-связями; π-связи между одними и теми же двумя атомами слабее, потому что они возникают в результате параллельного перекрытия, а множественные связи содержат одну или несколько π-связей (в дополнение к σ-связи).
3.
Удельное среднее расстояние связи — это расстояние с наименьшей энергией. На расстояниях, меньших расстояния связи, положительные заряды двух ядер отталкиваются друг от друга, и общая энергия увеличивается.
Связь: одна σ-связь и одна π-связь. Орбитали s заполнены и не перекрываются. Орбитали p перекрываются вдоль оси, образуя σ-связь, и бок о бок, образуя π-связь.
7.
Нет, две из p орбиталей (по одной на каждую N) будут ориентированы встык и образуют σ-связь.
9.
Гибридизация введена для объяснения геометрии связывающих орбиталей в теории валентных связей.
11.
В валентной оболочке углерода нет d орбиталей.
13.
треугольный плоский, sp 2 ; треугольная пирамидальная (одна неподеленная пара на А) sp 3 ; Т-образная (две неподеленные пары на А sp 3 d или (три одиночные пары на A) sp 3 d 2
15.
(a) Каждый S имеет изгибную (109 °) Геометрию, SP 3
(B) Bent (120 °), SP 2
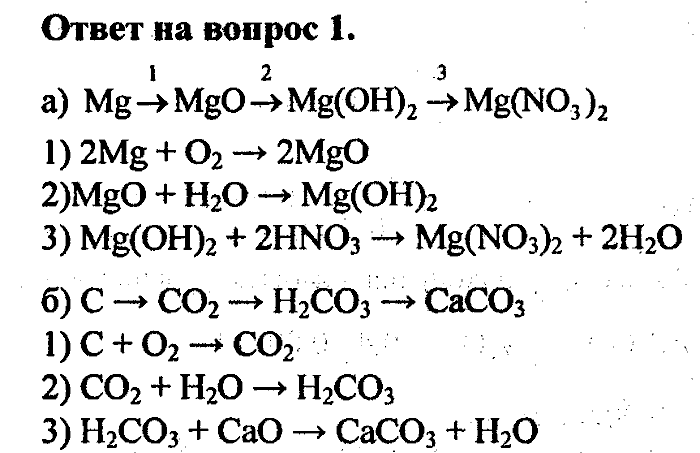 17
17 (а) XeF 2
(б)
(в) линейный (г) сп 3 г
19.
(а)
(б) Атомы Р, тригонально-пирамидальные; Атомы S, изогнутые, с двумя неподеленными парами; Атомы Cl, тригонально-пирамидальные; (c) Гибридизация по P, S и Cl во всех случаях
21.
Фосфор и азот могут образовывать sp 3 образуют три связи и удерживают одну неподеленную пару в PF 3 и NF 3 соответственно. Однако азот не имеет валентных d орбиталей, поэтому он не может образовывать набор гибридных орбиталей sp 3 d для связывания пяти атомов фтора в NF 5 . Фосфор имеет d орбиталей и может связывать пять атомов фтора с sp 3 d гибридными орбиталями в PF 5 .
Фосфор имеет d орбиталей и может связывать пять атомов фтора с sp 3 d гибридными орбиталями в PF 5 .
23.
Тройная связь состоит из одной σ-связи и двух π-связей. Связь σ прочнее связи π из-за большего перекрытия.
25.
(a)
(b) Терминальный атом углерода использует гибридные орбитали sp 3 , а центральный атом углерода гибридизован sp . (c) Каждая из двух π-связей образована перекрыванием орбитали 2 p углерода и орбитали азота 2 p .
27.
(а) sp 2 ; (б) sp ; (в) sp 2 ; (г) sp 3 ; (e)
29.
(a) sp 2 , делокализованный; (б) sp , локализованный; (c) sp 2 , делокализованный; (d) sp 3 , делокализованный
31.
Каждый из четырех электронов находится на отдельной орбитали и перекрывается с электроном на атоме кислорода.
33.
(a) Сходства: обе являются связывающими орбиталями, которые могут содержать максимум два электрона. Различия: σ-орбитали представляют собой непрерывные комбинации атомных орбиталей, тогда как π-орбитали образованы параллельным перекрытием орбиталей. (b) Сходства: оба являются квантово-механическими построениями, которые представляют вероятность нахождения электрона вокруг атома или молекулы. Отличий: ψ для атомной орбитали описывает поведение только одного электрона в каждый момент времени на основе атома. Для молекулы ψ представляет собой математическую комбинацию атомных орбиталей. (c) Сходство: обе орбитали могут содержать два электрона. Различия: связывающие орбитали приводят к тому, что два или более атома удерживаются вместе. Разрыхляющие орбитали дестабилизируют любую возникшую связь.
Для молекулы ψ представляет собой математическую комбинацию атомных орбиталей. (c) Сходство: обе орбитали могут содержать два электрона. Различия: связывающие орбитали приводят к тому, что два или более атома удерживаются вместе. Разрыхляющие орбитали дестабилизируют любую возникшую связь.
35.
Нечетное число электронов никогда не может быть спарено, независимо от расположения молекулярных орбиталей. Он всегда будет парамагнетиком.
Связывающие орбитали имеют электронную плотность в непосредственной близости от более чем одного ядра. Взаимодействие между связывающими положительно заряженными ядрами и отрицательно заряженными электронами стабилизирует систему.
39.
Спаривание двух связывающих электронов снижает энергию системы по сравнению с энергией несвязанных электронов.
41.
(a) H 2 порядок связи = 1, порядок связи h3+h3+ = 0,5, порядок связи h3-h3- = 0,5, самая сильная связь — H 2 ; (б) порядок связи O 2 = 2, порядок связи O22+O22+ = 3; порядок связи O22-O22- = 1, самая сильная связь O22+; O22+; (в) порядок связи Li 2 = 1, порядок связи Be2+Be2+ = 0,5, порядок связи Be 2 = 0, самая сильная связь Li2Li2; (d) порядок связи F 2 = 1, связь F2+F2+ порядок = 1,5, порядок связи F2-F2- = 0,5, самая сильная связь F2+; F2+; (e) N 2 порядок связи = 3, N2+N2+ порядок связи = 2,5, N2-N2- порядок связи = 2,5, самая сильная связь N 2
43.
(а) Н 2 ; (б) N 2 ; (в) О; (г) С 2 ; (д) В 2
45.
Да, атом фтора меньше, чем Li, поэтому атомы на орбите 2 s ближе к ядру и более стабильны.
47.

 Методы изучения химии
Методы изучения химии Строение пламени свечи
Строение пламени свечи Химические формулы
Химические формулы 47)
47) Оксиды
Оксиды 76)
76) Молярный объем газов
Молярный объем газов Растворы. Массовая доля растворенного вещества
Растворы. Массовая доля растворенного вещества Кислоты, их классификация и химические свойства
Кислоты, их классификация и химические свойства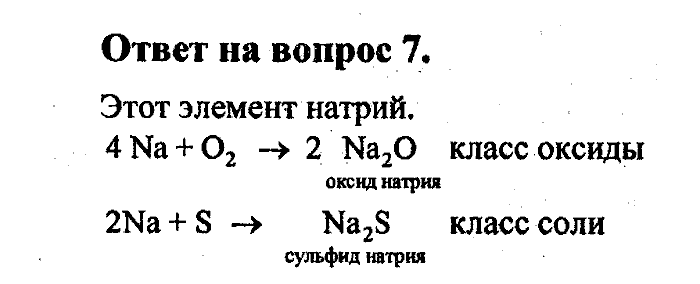 Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Строение электронных оболочек атомов
Строение электронных оболочек атомов Металлическая химическая связь
Металлическая химическая связь