ГДЗ практическая работа 2 химия 8 класс Габриелян, Остроумов
Решение есть!- 1 класс
- Математика
- Английский язык
- Русский язык
- Литература
- Окружающий мир
- 2 класс
- Математика
ГДЗ практическая работа 2 химия 7 класс Габриелян, Сладков
Решение есть!- 1 класс
- Математика
- Английский язык
- Русский язык
- Литература
- Окружающий мир
- 2 класс
- Математика
Практическая работа №2 «Изучение свойств соляной кислоты». | План-конспект урока по химии (9 класс) на тему:
| План-конспект урока по химии (9 класс) на тему:
Урок химии
9 класс
Тема: Практическая работа №2
«Изучение свойств соляной кислоты».
Тип урока — урок применения знаний, умений и навыков (практическая работа).
Цель
- образовательная: закрепить знания о свойствах соляной кислоты; формировать навыки практической работы с реактивами, совершенствовать умения обращаться с кислотами; научить способам распознания соляной кислоты и ее солей; составлять уравнения реакций; наблюдать и делать выводы;
- развивающая: совершенствовать навыки работы с химической посудой; развивать коммуникативные навыки работы в парах; развивать познавательный интерес к химии;
- воспитательная: воспитывать ответственность, самостоятельность при выполнении практической работы, формировать коммуникативные качества обучающихся при организации работы в парах; формировать познавательный интерес, ценностное отношение к химии как науке и учебному предмету.

Планируемые результаты: уметь применять полученные теоретические знания о свойствах соляной кислоты в практической работе, проводить опыты по осуществлению реакций в соответствии с правилами безопасного обращения с химическими веществами и правилами пользования химической посудой, описывать свойства веществ и наблюдения в ходе эксперимента.
Оборудование и реактивы: штатив с пробирками, раствор соляной кислоты, лакмус, гранула цинка, медная проволока, сульфат меди (II), гидроксид натрия, карбонат натрия, нитрат серебра.
Периодическая система химических элементов Д.И. Менделеева, таблица растворимости, инструкционная карта практической работы (приложение 1), раздаточный материал инструкция по ТБ «Техника безопасности при работе с кислотами».
Методы обучения: объяснительно-иллюстративные, словесные, практические, частично-поисковые, исследовательские.
Структура урока
- Организационный этап.
- Мотивация учебной деятельности.

- Постановка цели и задач урока. Совместное планирование учебной деятельности.
- Актуализация опорных знаний и деятельности учащихся, необходимых для творческого решения задач.
- Самостоятельное выполнение практической части работы и текущее инструктирование учителя.
Составление отчета. Контроль, взаимоконтроль в процессе выполнения работы.
- Подведение итогов урока. Проведение рефлексии.
- Домашнее задание и инструктаж по его выполнению.
Ход урока
1. Организационный этап.
Приветствие. Определение готовности обучающихся к уроку. Позитивный настрой на урок.
На каждом столе набор химических реактивов и оборудования: штатив с пробирками, раствор соляной кислоты, лакмус, гранула цинка, медная проволока, оксид меди (II), сульфат меди (II), гидроксид натрия, карбонат натрия, нитрат серебра.
Обучающиеся оформляют практическую работу в тетрадях для практических работ.
2. Мотивация учебной деятельности.
Зайдя в класс, вы увидели, что сегодня он превратился в большую химическую лабораторию. Представьте, что вам, как ее научным сотрудникам, поручили провести ответственную исследовательскую работу. Надеюсь, что вы покажите себя серьезными и ответственными работниками.
Девиз урока: “Химик требуется не такой, который лишь из одного чтения книг понял сию науку, но который собственным искусством в ней прилежно упражнялся…” М.В. Ломоносов.
3. Постановка цели и задач урока. Совместное планирование учебной деятельности.
Напомните, пожалуйста, какое химическое соединение мы изучали на прошлом уроке? Правильно, соляную кислоту, ее свойства, способы получения. Поэтому тема сегодняшнего урока: «Практическая работа по теме «Изучение свойств соляной кислоты». Определяем цели урока, записываем их в тетрадь. Зная цели, составляем вместе план урока.
4. Актуализация опорных знаний.
Перед тем, как начать практическую работу проведем небольшую химическую разминку. Вспомним, какие физические и химические свойства соляной кислоты. Проверим домашнее задание.
Проверим домашнее задание.
На производстве перед проведением испытаний, исследований обязательно проводят с сотрудниками инструктаж по охране труда.
Сегодня мы тоже, как научные сотрудники химической исследовательской лаборатории проведем инструктаж по ТБ перед проведением практической работы, используя инструкцию. Обучающиеся повторяют правила безопасной работы с кислотами и щелочами, нагревательными приборами. В тетрадях учащиеся делают запись «С правилами ТБ при работе с кислотами и щелочами, нагревательными приборами ознакомлен(а)».
- Самостоятельное выполнение практической части работы и текущее инструктирование учителя. Составление отчета.
Дорогие друзья! На каждом столе есть инструкционная карта с четкой инструкцией по выполнению практической работы. Напоминаю требования к оформлению результатов проведенных исследований в тетрадях: следует кратко записать, что делали, что наблюдали, записать соответствующие уравнения реакций в молекулярном и ионных видах, сделать вывод.
В ходе практической работы буду осуществлять контроль за вашей деятельностью, за соблюдением техники безопасности. По завершению практической работы представьте результаты своих научных исследований на проверку.
Ход работы:
Задание 1. В пробирку налейте 1 мл соляной кислоты и добавьте 1-2 капли лакмуса. Какие изменения с раствором происходят? Запишите свои наблюдения. Появление розово-красной окраски раствора.
Задание 2. В две пробирке налейте по 1 мл соляной кислоты. В первую пробирку добавьте гранулу цинка, а во вторую – медную проволоку. Что наблюдаете? Со всеми ли металлами реагирует соляная кислота? Составьте уравнения реакций в молекулярном и ионном видах, протекающих между соляной кислотой и указанными металлами.
Соляная кислота реагирует с цинком, в результате этого взаимодействия выделяется газ – водород. С медью соляная кислота не реагирует, т.к. медь является неактивным металлом.
Zn +2HCl = ZnCl2 + h3↑
Zn + 2H+ + 2Cl — = Zn2+ + 2Cl — + h3↑
Zn + 2H+ = Zn2+ + h3↑
Задание 3. К свежеприготовленному гидроксиду меди (II) добавьте раствор соляной кислоты. Что наблюдаете? Как объяснить образование в пробирке раствора синего цвета? Составьте уравнения реакций в молекулярном и ионном видах.
К свежеприготовленному гидроксиду меди (II) добавьте раствор соляной кислоты. Что наблюдаете? Как объяснить образование в пробирке раствора синего цвета? Составьте уравнения реакций в молекулярном и ионном видах.
Приготовление гидроксида меди (II): к раствору гидроксида натрия добавляют немного раствора сульфата меди (II).
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
Cu2+ + SO42- + 2Na+ + 2OH — = 2Na+ + SO42- + Cu(OH)2↓
Cu2++ 2OH- = Cu(OH)2↓
Образуется синий желеобразный осадок.
При взаимодействии соляной кислоты со свежеприготовленным раствором гидроксида меди (II) происходит растворение осадка и образование раствора хлорида меди (II) синего цвета.
Cu(OH)2↓ + 2HCl = 2h3O + CuCl2
Cu(OH)2↓ + 2H+ + 2Cl — = 2h3O + Cu2+ + 2Cl –
Cu(OH)2↓ + 2H+= 2h3O + Cu2+
Задание 4. В пробирку налейте 1 мл раствора соляной кислоты и добавьте раствор карбоната натрия. Что наблюдаете? Как объяснить выделение газа при данном взаимодействии? Составьте уравнения реакций в молекулярном и ионном видах.
При взаимодействии соляной кислоты с раствором карбоната натрия происходит выделение углекислого газа.
Na2CO3 + 2HCl = h3O + CO2↑ + 2NaCl
2Na+ + CO32- + 2H+ + 2Cl — = h3O + CO2↑ + 2Na+ + 2Cl –
2H+ + CO32- = h3O + CO2↑
Задание 5. В пробирку налейте 1 мл раствора соляной кислоты и добавьте несколько капель раствора нитрата серебра. Что наблюдаете? Аналогично в пробирку с раствором хлорида натрия добавить несколько капель раствора нитрата серебра. Напишите уравнения в молекулярном и ионном видах. Ответьте на вопрос, что является реактивом на соляную кислоту.
Реактивом на соляную кислоту и ее соли является раствор нитрата серебра, в результате реакции образуется белый творожистый осадок хлорида серебра.
HCl + AgNO3 = AgCl↓ + HNO3
H+ + Cl — + Ag+ + NO3- = AgCl↓ + H+ + NO3-
Ag+ + Cl — = AgCl↓
Во время проведения практической работы учитель наблюдает за действиями учащихся, помогает в случае необходимости. Результаты опытов обговариваются. Учащиеся в тетрадях записывают вывод.
Учащиеся в тетрадях записывают вывод.
После окончания практической работы учащиеся должны привести рабочее место в порядок.
- Домашнее задание и инструктаж по его выполнению.
Повторить §35.
Подготовить сообщение (на выбор): 1) о применении соляной кислоты;
2) из истории открытия соляной кислоты.
- Подведение итогов урока. Проведение рефлексии.
Уважаемые сотрудники исследовательской лаборатории! Вы сегодня на славу потрудились. Работали дружно, слаженно. Результаты проведенных вами исследований вы сдали на проверку. Ответьте, пожалуйста на вопросы:
Что открыли, узнали на уроке? Почему было трудно? Оправдались ли ваши ожидания от урока? Над чем заставил задуматься урок?
Всем спасибо! Хорошего настроения!
Приложение 1
Цель: Исследовать химические свойства соляной кислоты.
Оборудование и реактивы: пробирки, соляная кислота, лакмус, Mg, Сu, Cu(OH)2, NaOH, CuSO4 , Nа2CO3, NаCl, AgNO3.
С правилами ТБ ознакомлен (а) (подпись).
Ход работы.
Опыт № 1. Действие индикатора на соляную кислоту HCl.
В пробирку с соляной кислотой добавьте 1-2 капли лакмуса.
Что наблюдаете? Сделайте вывод.
Опыт № 2. Взаимодействие соляной кислоты HCl с металлами.
В пробирку с соляной кислотой положите гранулу цинка, а в другую — кусочек медной проволоки.
Что наблюдаете?
Со всеми ли металлами реагирует соляная кислота? Сделайте вывод.
Составьте уравнение реакции.
Опыт № 3. Взаимодействие соляной кислоты HCl с основаниями.
К свежеприготовленному раствору гидроксида меди прилейте соляную кислоту.
Что наблюдаете? Сделайте вывод.
Составьте уравнение реакции в молекулярном, полном и сокращенном ионном виде.
Справка. Для получения гидроксида меди Cu(OH)2 к раствору CuSO4 прилить щелочь NaOH, при этом образуется осадок голубого цвета Cu(OH)2:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
Опыт № 4.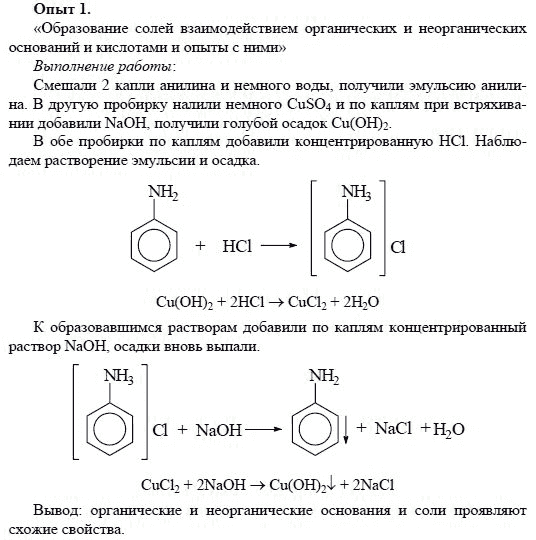 Взаимодействие соляной кислоты HCl с солями.
Взаимодействие соляной кислоты HCl с солями.
В пробирку с карбонатом натрия прилейте соляную кислоту.
Что наблюдаете? Сделайте вывод.
Составьте уравнение реакции в молекулярном, полном и сокращенном ионном виде.
Опыт № 5. Распознавание соляной кислоты HCl и ее солей.
(Качественная реакция на хлорид-ионы)
В одну пробирку с соляной кислотой, в другую пробирку с раствором хлорида натрия добавьте по нескольку капель раствора нитрата серебра.
Что наблюдаете? Сделайте вывод.
Напишите уравнения проведенных реакций в молекулярном виде.
Укажите, как можно отличить: а) соляную кислоту от других кислот, б) хлориды от других солей
Почему вместо раствора нитрата серебра(I) можно также использовать раствор нитрата свинца(II)?
Сделайте общий вывод.
WAEC Химический практический образец 2020 Ответы
WAEC Chemistry Practical Answers 2020 вышел — см. Образец для химического титрования здесь.
Доклад Waec Chemistry Practical 2020 для SSCE будет написан в четверг, 3 сентября, с 14:00 до 15:30. Сегодняшняя статья — это практическая альтернатива Waec Chemistry A.
Сегодняшняя статья — это практическая альтернатива Waec Chemistry A.
Мы сделали этот пост, чтобы показать прибор, практический образец химии Waec, графики и расчеты, которые использовались в вопросах и программе практического экзамена по химии.
Здесь мы предоставим вам прошлые вопросы и материалы по практической химии Waec 2020, которые будут использоваться при подготовке к экзаменам. Читайте ответы ниже.
WAEC Chemistry Practical 2020 Аппарат.
Следующее оборудование и материалы потребуются каждому кандидату на практическую работу по WEC-химии 2020;
(b) одна пипетка объемом 20 см³ или 25 см³.
(c) обычный аппарат для титрования.
(d) следующие реагенты;
(i) разбавленный раствор гидроксида натрия.
(ii) разбавленная соляная кислота.
(iii) разбавленный раствор триоксонитрата (v) кислоты
(iv) раствор триоксонитрата серебра (v).
(v) раствор хлорида бария.

(vi) водный аммиак.
(vii) известковая вода.
(viii) красная и синяя лакмусовая бумага.
(ix) разбавленная тетраоксосульфат (vi) кислота.
- Каждому кандидату должна быть предоставлена следующая информация, где n — порядковый номер кандидата.
(a) 150 см³ раствора триоксосульфата натрия (vi) в закупоренной колбе или бутылке с надписью «An».Все они должны быть одинаковыми с содержанием 6,0 г Na2S2O3 на дм3 раствора. - 150 см³ йода в растворе йодида калия в закупоренной колбе или бутылке с надписью «Bn». Все они должны быть одинаковыми с содержанием 2,5 г I2 и 1,67 г KI на дм3 раствора.
- Один шпатель, заполненный однородной смесью NaCl и CuCO3 в бутылке для образцов с надписью «Cn». Компоненты смеси должны быть в соотношении 1: 2 по массе.
Практические вопросы и ответы WAEC по химии.
1. А — раствор кислоты с концентрацией 0,100 моль дм-3. Б — раствор КОН, содержащий 2,8 г на 500 см3.
(a) Поместите A в бюретку и оттитруйте ее по 25,0 см3 части B, используя метиловый оранжевый в качестве индикатора. Повторите титрование для получения стабильных титров. Сведите свои показания в таблицу и рассчитайте средний объем используемого A.
(b) На основе ваших результатов и информации, представленной выше, рассчитайте:
(i) количество молей кислоты в среднем титре;
(iii) мольное отношение кислоты к основанию в реакции
[H = 1.00, O = 16,0, K = 39,0]
ANS: (a) ответ на титрование в ближайшее время.
(b) (i) число молей кислоты = 0,100 x V A
1000
= X моль (ов) [3sig. Инжир для оценки]
1000 см3 содержит 0,100 моль (с)
VA будет содержать 0,100 x V A
1000
= X моль [3 сиг.Рис. Для оценки]
(ii) Количество молей КОН в B
500 см3 B содержит 2,8 г KOH
1000 см3 B будет содержать 2,8 x 1000 = 5,6 КОН
500
Молярная масса KOH = 39 + 16 + 1 или 56 гмоль -1
Концентрация B = 5,6 = 0,100 моль дм-3
56
(iii) Мольное отношение кислоты к основанию = X: Y до ближайшего целочисленного отношения.
2. C представляет собой смесь двух солей. Выполните следующие упражнения на C. Запишите свои наблюдения и определите выделившийся газ (ы). Сформулируйте вывод, сделанный по результатам каждого теста.
(a) Поместите весь C в трубку для кипячения и добавьте около 5 см3 дистиллированной воды. Тщательно перемешайте и профильтруйте. Сохраните и остаток, и фильтрат.
(b) Примерно к 2 см3 фильтрата добавьте несколько капель Pb (NO3) 2 (водн.) ‑ Вскипятите смесь и дайте ей остыть.
(c) (i) Поместите остаток в пробирку и добавьте разбавленную HNO3.Встряхните смесь и разделите раствор на две части.
(ii) К первой порции из (c) (i) добавить NaOH (водн.) По каплям, а затем в избытке.
(iii) Ко второй части из (c) (i) добавляют по каплям водный раствор аммиака и его избыток.
ОТВЕТ:
ТЕСТ | НАБЛЮДЕНИЕ | ВЫВОД |
а) C + вода, смесь перемешивают | Частично растворяется / растворим Бесцветный фильтрат | C содержит растворимые и нерастворимые соли |
б) Фильтрат + Pb (NO3) 2 (водн. | Образовался белый осадок | Cl-, SO42- или CO32. |
c) (i) Остаток + разбавленная HNO3 | Вздутие / пузырьки / выделение газа бесцветный газ без запаха. Газ превращается в известковую воду молочного цвета. | CO2 выделился из CO32- |
(ii) Раствор из (c) (i) + NaOH (водн.) По каплям, затем в избытке | Образовался белый студенистый ppt.Осадок растворяется | Zn2 + или A13 + Zn2 + или A13 + |
(iii) Раствор из (c) (i) + HN3 (водн.) В каплях, затем в избытке | Белый студенистый. | Zn2 + или A13 + Zn2 + подтверждено |
3. (a) Кратко объясните наблюдения в каждом из следующих процессов:
(i) когда оксид углерода (IV) барботируется через известковую воду, он становится молочным, но молочный цвет исчезает, когда газ барботируют в течение некоторого времени. много времени;
(b) (i) Что такое первичный стандартный раствор?
(ii) Рассчитайте массу триоксокарбоната (IV) натрия, необходимую для приготовления 250 см3 раствора 0,15 м-3.
[Na = 23,0; О = 16,0; C = 12,0]
(c) Назовите один газ, который может быть собран с помощью:
(i) вытеснения воздуха вверх;
(ii) смещение воздуха вниз.
ANS: (a) (i): Образование нерастворимого CaCO3 является причиной молочности продукта, когда CO2 барботируется через известковую воду, тогда как исчезновение молочности происходит из-за образования растворимого Ca (HCO3) 2.
Известковая вода становится молочной из-за CO2, потому что образуются CaCO3 / CaCO3 (ы). Молочность исчезает, когда избыток CO2 реагирует с CaCO3 в водной среде, образуя растворимый Ca (HCO3) 2 / Ca (HCO3) 2 (водн.).
(ii) Гидроксид кальция не является амфотерным. Не реагирует с щелочным NaOH, в то время как гидроксид свинца (II) является амфотерным, поэтому реагирует с избытком NaOH.
(b) (i) Первичный стандартный раствор — это раствор, концентрация которого известна и может использоваться для стандартизации другого раствора.
(ii) M (Na2CO3) = 106 гмоль-1
м (Na2CO3) = C x M x V
= 0.15 x 106 x 0. 25
= 3. 98 г
(c) (i) Оксид углерода (IV), оксид серы (IV), хлористый водород, кислород, оксид азота (IV), хлор, сероводород.
(ii) Аммиак, кислород, водород, метан.
Добавьте эту страницу в закладки и следите за обновлениями. Также задайте свои вопросы, разместив комментарий ниже.
Поделись любовью — поделись этим с друзьями
CHEM 2530 — Экологическая и аналитическая химия II
CHEM 2530 — Экологическая и аналитическая химия II
North Terrace Campus — 1 семестр — 2021 г.
202120202012017201620152014
Химический анализ — как количественный, так и видообразовательный — является одним из наиболее ценных профессиональных навыков квалифицированных химиков.Этот курс направлен на то, чтобы вооружить студентов рабочими знаниями и набором практических навыков для профессиональной аналитической химии и ее применения в ряде экологических систем и промышленных приложений. Студенты будут обучены методам, используемым профессиональными химиками для определения химического состава и анализа на следовые соединения, которые являются ключевыми для рассматриваемых экологических систем. Основы аналитической строгости будут рассмотрены и развиты как в теории, так и на практике.Курс установит правильное понимание химии биосферы и воздействия природных и антропогенных явлений на локальную и глобальную окружающую среду. Изучаются химический состав атмосферы, суши, реки и океана и их взаимодействия, приводящие к изменению климата и другим условиям окружающей среды.
Сведения о курсе
Код курса ХИМ 2530 Курс Экологическая и аналитическая химия II Координационная группа Школа физических наук Срок Семестр 1 Уровень Бакалавриат Расположение / с North Terrace Campus Шт. 3 Связаться До 7.5 часов в неделю Доступно для обучения за границей и обмена Y Предварительные требования CHEM 1100 и CHEM 1200 или CHEM 1101, CHEM 1201 и CHEM 1312. Другие студенты могут обратиться к главе химического факультета с просьбой об освобождении от налогов Описание курса Химический анализ — как количественный, так и видообразовательный — является одним из самых ценных профессиональных навыков квалифицированных химиков.  Этот курс направлен на то, чтобы вооружить студентов рабочими знаниями и набором практических навыков для профессиональной аналитической химии и ее применения в ряде экологических систем и промышленных приложений. Студенты будут обучены методам, используемым профессиональными химиками для определения химического состава и анализа на следовые соединения, которые являются ключевыми для рассматриваемых экологических систем. Основы аналитической строгости будут рассмотрены и развиты как в теории, так и на практике.
Этот курс направлен на то, чтобы вооружить студентов рабочими знаниями и набором практических навыков для профессиональной аналитической химии и ее применения в ряде экологических систем и промышленных приложений. Студенты будут обучены методам, используемым профессиональными химиками для определения химического состава и анализа на следовые соединения, которые являются ключевыми для рассматриваемых экологических систем. Основы аналитической строгости будут рассмотрены и развиты как в теории, так и на практике.Курс установит правильное понимание химического состава биосферы и воздействия природных и антропогенных явлений на локальную и глобальную окружающую среду. Изучаются химический состав атмосферы, суши, реки и океана и их взаимодействия, приводящие к изменению климата и другим условиям окружающей среды.
Курс
Координатор курса: Доцент Так Ки
A / Prof Tak W. Ки ([email protected]) для лекций и профессора MyUni
Ки ([email protected]) для лекций и профессора MyUni
Кристиана Дунана ([email protected]) для практических занятийРасписание занятий
Полное расписание всех мероприятий для этого курса доступно в Планировщике курса.
Результаты обучения
По завершении этого курса студенты должны уметь:1 демонстрируют знание и понимание принципов количественного анализа и основополагающих принципов устойчивого использования
химических веществ в различных количественных химических контекстах2 разрабатывать аналитические решения различных химических проблем, выявленных в контексте приложений; критически анализировать и оценивать количественную и качественную химическую информацию 3 в составе команды или индивидуально разрабатывать, проводить, анализировать и интерпретировать результаты эксперимента и эффективно сообщать о них в письменных отчетах
и других форматах4 описать и объяснить, как химический анализ позволил / продолжает позволять человечеству понять и смягчить его влияние на мир природы, где оно должно выжить. 
5 получить понимание и оценку того, как фундаментальная аналитическая химия влияет на жизнь, окружающую среду и промышленные процессы Атрибуты выпускника университета
Этот курс предоставит студентам возможность развить атрибуты выпускника, указанные ниже:
Атрибут выпускника университета Результаты обучения по курсу Глубокие знания дисциплины - , основанные на передовых исследованиях, поддерживаемые на протяжении всей программы обучения
- , полученные в результате личного взаимодействия с активными преподавателями-исследователями, с 1 года
- аккредитованы или подтверждены в соответствии с национальными или международными стандартами ( для соответствующих программ)
1,2,4 Критическое мышление и решение проблем - с опорой на методы исследования и строгость
- на основе эмпирических данных и научного подхода к развитию знаний
- продемонстрировано посредством соответствующей и актуальной оценки
1-5 Командные навыки и коммуникативные навыки - , развитые на основе SGDE, с его помощью и посредством SGDE
- , отточенные посредством оценки и практики на протяжении всей программы обучения
- поощряются и ценятся во всех аспектах обучения
1,3,4 Карьера и готовность к руководству - технологическая смекалка
- профессионал и, где это уместно, полностью аккредитован
- дальновидное мышление и хорошо информированный
- протестировано и подтверждено опытом работы
2,3,5 Межкультурная и этическая компетентность - опытный в работе с другими культурами
- комфортно работать с разными национальностями и социальными контекстами
- способный определять и вносить свой вклад в достижение желаемых социальных результатов
- демонстрируется обучением за рубежом или пониманием коренных народов знания
3,4,5 Самосознание и эмоциональный интеллект - Способность к саморефлексии и готовность к самооценке
- Открытость для объективной и конструктивной обратной связи от руководителей и коллег
- способна решать сложные социальные ситуации, разрядить конфликт и участвовать в целенаправленных дебатах
3,4,5 Рекомендуемые ресурсы
Химия окружающей среды (Бэрд и Канн, 5-е изд. , W.H. Фримен.
, W.H. Фримен.
Можно приобрести в UniBooks. (Предыдущие издания также подходят, и некоторые копии могут быть доступны из вторых рук.) Экзамен за семестр 1 предполагает знакомство с указанными разделами учебника.Количественный химический анализ (Harris, 8-е издание, WH Freeman)
Можно приобрести в UniBooks.Онлайн-обучение
MyUni: Учебные материалы и документация курса будут размещены на веб-сайте MyUni (http: // myuni.adelaide.edu.au/).
Ресурсы по математике
Учебный центр математики (MLC) помогает всем студентам изучать и использовать математику, которая им нужна в университете. MLC предлагает семинары, практикумы, онлайн-ресурсы и печатные ресурсы. Кроме того, в Hub Central с 10:00 до 16:00 с понедельника по пятницу во время учебных недель работает служба поддержки.Для получения дополнительной информации посетите http://www.
 adelaide.edu.au/mathslearning/
adelaide.edu.au/mathslearning/Для получения справки по математике по химии посетите http://www.adelaide.edu.au/mathslearning/resources/chem
Режимы обучения и преподавания
- Лекции 36 занятий по 1 часу (3 в неделю)
- Обучающие программы 12 занятий по 1 часу (1 в неделю)
- Практические занятия 10 х 4-часовых занятий (включая ознакомительную лабораторную сессию)
- Презентация на 6-й или 12-й неделе
Рабочая нагрузка
Приведенная ниже информация предоставляется в качестве руководства, чтобы помочь студентам надлежащим образом выполнить требования курса.
Студент, зачисленный на курс из 3 частей, подобный этому, должен рассчитывать тратить в среднем 12 часов в неделю на необходимые исследования.
 Это включает в себя как формальное время контакта, необходимое для курса (например, лекции и практические занятия), так и время без контакта (например, чтение и повторение).
Это включает в себя как формальное время контакта, необходимое для курса (например, лекции и практические занятия), так и время без контакта (например, чтение и повторение).Сводка учебных мероприятий
Методы аналитической химии (9 лекций + 3 учебных курса)
- Этот раздел знакомит студентов с широким спектром инструментальных методов аналитической химии, включая электрохимические, спектроскопические и рентгеновские методы, а также инструменты, а также основные критические методы для разделения аналитов, особенно хроматографии.
- Атмосфера, почвенная / земная химия (9 лекций + 3 учебных курса ) — Изучаются химические составы атмосферы, суши, реки и океана, а также их взаимодействия, приводящие к изменению климата и другим условиям окружающей среды. Изучаются природные химические циклы, имеющие важное экологическое значение, такие как циклы углерода, азота, кислород-озон, фосфор и сера.

- Химия воды (9 лекций + 3 учебных курса) — Химическое воздействие на окружающую среду человеческой деятельности, такой как сельское хозяйство, горнодобывающая промышленность и другие отрасли, а также использования ископаемого топлива и ядерного топлива, рассматривается как в общих чертах, так и на основе тематических исследований.
- Практикующий химик-аналитик (9 лекций + 3 учебных курса) — Студенты будут ознакомлены с основополагающими принципами количественного химического анализа, валидации и обеспечения качества, включая: экспериментальный план, экспериментальные ошибки и статистику, калибровку, химиометрию, этику .
4-часовое занятие в первую неделю посвящено безопасным методам работы в лаборатории аналитической химии с упором на управление рисками, оценку химического риска и ознакомление с лабораторией.Затем последуют три недели занятий на основе навыков, посвященных стандартам и анализу ошибок, аналитическим методологиям и методам, сбору данных и обработке данных с помощью разнообразного программного обеспечения. Остальные занятия позволят студентам реализовать эти навыки, подготовить стандарты и разработать аналитические методологии, качественно и количественно оценить результаты и поместить эти анализы в более широкий экологический контекст. Будет обеспечено обучение и руководство по распространению результатов этих расследований в различных форматах.
Остальные занятия позволят студентам реализовать эти навыки, подготовить стандарты и разработать аналитические методологии, качественно и количественно оценить результаты и поместить эти анализы в более широкий экологический контекст. Будет обеспечено обучение и руководство по распространению результатов этих расследований в различных форматах.Специальные требования к курсу
Посещение всех запланированных практических занятий по химии обязательно.
Политика Университета в отношении оценивания программ курсовой работы основана на следующих четырех принципах:
- Оценка должна поощрять и укреплять обучение.
- Оценка должна позволять выносить обоснованные и справедливые суждения об успеваемости учащихся.
- Практика оценивания должна быть справедливой и равноправной по отношению к учащимся и давать им возможность продемонстрировать то, чему они научились.

- Оценка должна соответствовать академическим стандартам.
Сводка оценки
Задание на оценку Тип оценки Процент общей оценки для выставления оценок # Препятствие Да или Нет # Оцениваемые / достигнутые результаты Примерные сроки
аттестации(неделя периода обучения)
Презентации Формирующий и Суммативный 10% № 1, 3,5 6 или 12 неделя Практические навыки и научное общение Формирующий и Суммативный 30% № 1, 3, 4 Примерно еженедельно в течение 2-5 недель; раз в две недели с 6 по 11 неделю Экзамен Суммативное 60% Да (45%) 1, 2, 4 Экзаменационный период Требования, связанные с оценкой
Практическая работа является обязательной — сюда входит посещение, проведение необходимой экспериментальной работы, присутствие на собеседовании с демонстратором (при необходимости) и представление лабораторных отчетов. Результаты обучения по этому курсу в значительной степени зависят от лабораторного опыта и практики. Таким образом, пропуск какого-либо практического занятия в семестре приведет к тому, что для курса будет выставлена оценка FAIL. Учащимся, не посещающим занятия по медицинским причинам или из соображений сострадания, будет предоставлена возможность восполнить пропущенные практические занятия.
Результаты обучения по этому курсу в значительной степени зависят от лабораторного опыта и практики. Таким образом, пропуск какого-либо практического занятия в семестре приведет к тому, что для курса будет выставлена оценка FAIL. Учащимся, не посещающим занятия по медицинским причинам или из соображений сострадания, будет предоставлена возможность восполнить пропущенные практические занятия.Для прохождения этого курса студенты должны набрать минимум 45% для сдачи экзамена и присутствовать на всех практических занятиях. Студентам, получившим итоговую оценку по курсу не менее 45%, но не набравшим минимум 45% для экзамена, может быть предложен дополнительный академический экзамен в течение периода замены / дополнительной оценки в соответствии с Модифицированными процедурами оценки курсовой работы. .
Сведения об оценке
Презентация 10%
Эта презентация длится 10 минут и проводится парой студентов (средняя продолжительность презентации для каждого студента составляет 5 минут). Студенты индивидуально оцениваются сотрудниками и их сверстниками.
Студенты индивидуально оцениваются сотрудниками и их сверстниками.Практические навыки и научное общение 30%
4-часовая сессия в первую неделю посвящена безопасным методам работы в лаборатории аналитической химии с упором на управление рисками, оценку химических рисков и ознакомление с лабораторией.Затем последуют три недели занятий на основе навыков, посвященных стандартам и анализу ошибок, аналитическим методологиям и методам, сбору данных и обработке данных с помощью разнообразного программного обеспечения. Остальные занятия позволят студентам реализовать эти навыки, подготовить стандарты и разработать аналитические методологии, качественно и количественно оценить результаты и поместить эти анализы в более широкий экологический контекст. Будет обеспечено обучение и руководство по представлению результатов этих расследований в письменных отчетах объемом около 500 слов в различных форматах.
В течение семестра может быть предложена возможность восполнить максимум одно пропущенное практическое занятие. У студентов будет множество возможностей продемонстрировать свои навыки в течение семестра. Студенты должны как можно скорее связаться с координатором курса, чтобы обсудить макияж.
У студентов будет множество возможностей продемонстрировать свои навыки в течение семестра. Студенты должны как можно скорее связаться с координатором курса, чтобы обсудить макияж.Заключительный экзамен 60%
Экзамен длится 3 часа и охватывает все содержание курса.Представление
Подача заданных работ Обложки должны быть заполнены и прикреплены ко всем представленным работам.Инструкции по подаче работы и титульные листы будут предоставлены на MyUni.
Продление сроков выполнения заданий по оценке По разумным причинам может быть разрешено продление сроков выполнения заданий по оценке. Такие ситуации будут включать в себя сострадательные и медицинские основания серьезности, которые оправдали бы назначение дополнительного обследования. При запросе о продлении должны быть представлены доказательства оснований.
 Студенты должны подать заявку на продление к Координатору курса до наступления срока выполнения задания.Продления не будут предоставлены из-за неправильного распределения времени. Бланк заявки на продление оценки можно получить по адресу: http://www.sciences.adelaide.edu.au/current/
Студенты должны подать заявку на продление к Координатору курса до наступления срока выполнения задания.Продления не будут предоставлены из-за неправильного распределения времени. Бланк заявки на продление оценки можно получить по адресу: http://www.sciences.adelaide.edu.au/current/Несвоевременная подача оценок Если продление не подавалось или не было предоставлено, то будет применяться штраф за несвоевременную подачу оценок. Будет применен штраф в размере 10% от стоимости задания за каждый календарный день, который просрочен (т. Е. Выходные считаются за 2 дня), но не более 50% имеющихся оценок.Это означает, что задание, которое задерживается на 5 или более дней без утвержденного продления, может получить максимум 50% оценки.
Оценка курса
баллов за вашу работу на этом курсе будут выставляться в соответствии со следующей схемой:
M10 (Схема оценок курсовых работ) Оценка Марка Описание FNS Номер ошибки F 1-902 50-64 Проходной C 65-74 Кредит D 75-84 Различие HD 8510-100 9011 Высокая 8510-100 9011 CN Продолжение NFE Без формальной проверки RP Ожидаемый результат Более подробную информацию об оценках / результатах можно получить на экзаменах.
Доступны
дескриптора оценок, которые обеспечивают общее руководство по стандарту работы, который ожидается на каждом уровне. Более подробная информация представлена в разделе «Оценка программ курсовой работы».
Окончательные результаты этого курса будут доступны через Access Adelaide.
Университет уделяет большое внимание подходам к обучению и преподаванию, которые улучшают опыт студентов. Обратная связь от студентов запрашивается различными способами, включая постоянное взаимодействие с персоналом, использование онлайн-форумов и использование опросов по опыту обучения и преподавания студентов (SELT), а также опросов GOS и обзоров программ.
SELTявляются важным источником информации для индивидуальной педагогической практики, принятия решений об обязанностях преподавателя, а также для разработки учебных программ и курсов. Они позволяют университету оценить, насколько эффективно его учебная среда и методы преподавания способствуют вовлечению студентов и результатам обучения. В соответствии с действующей политикой SELT (http://www.adelaide.edu.au/policies/101/) SELT курса обязательна и должна проводиться в конце каждого семестра / семестра / триместра для каждого предлагаемого курса.Отзывы о проблемах, поднятых в ходе опросов SELT, доступны для зачисленных студентов через различные ресурсы (например, MyUni). Кроме того, доступны агрегированные данные SELT курса.
В этом разделе содержатся ссылки на соответствующие политики и руководства в отношении оценивания — все политики университета.
Напоминаем студентам, что для поддержания академической целостности всех программ и курсов университет придерживается подхода абсолютной нетерпимости к студентам, предлагающим деньги или товары или услуги значительной ценности любому сотруднику, который участвует в их обучении или оценке.Студенты, предлагающие лекторам, наставникам или профессиональному персоналу что-либо большее, чем небольшой знак признательности, абсолютно неприемлемы ни при каких обстоятельствах. Сотрудники обязаны сообщать обо всех таких инцидентах своему руководителю / менеджеру, который направляет их для принятия мер в соответствии с дисциплинарными процедурами университета.
Университет Аделаиды обязуется регулярно пересматривать курсы и программы, которые он предлагает студентам.Таким образом, Университет Аделаиды оставляет за собой право прекращать или изменять программы и курсы без предварительного уведомления. Пожалуйста, прочтите важную информацию, содержащуюся в заявлении об отказе от ответственности.
Калькулятор с дополнением до двух
Как работать с отрицательными числами в двоичной системе? — представление 2-х дополнений
В двоичной системе все числа представляют собой комбинацию двух цифр: 0 или 1 .Каждая цифра соответствует степени 2, начиная справа.
Например, 12 в двоичном формате это 1100 , так как 12 = 8 + 4 = 1 * 2³ + 1 * 2² + 0 * 2¹ + 0 * 2⁰ (в экспоненциальном представлении). Расширенная версия двоичной системы — это шестнадцатеричная система (в которой используется основание 16 вместо 2). Последняя частота используется во многих компьютерных программах и системах.
Изучение двоичной системы приводит ко многим естественным вопросам — а как насчет отрицательных чисел в двоичной системе? Или как вычесть двоичные числа? Поскольку мы можем использовать только 1 , чтобы показать, что присутствует что-то , или 0 , чтобы обозначить отсутствие этой вещи , существует два основных подхода:
Представление с дополнением до двух , или, другими словами, обозначение со знаком — первый бит сообщает о знаке.Принято считать, что число с ведущим числом
1является отрицательным , а ведущее число0обозначает положительное значение . В 8-битном представлении мы можем записать любое число от -128 до 127. Название происходит от того факта, что отрицательное число — это два дополнения от положительного.Беззнаковая запись — представление, поддерживающее только положительные значения. Его преимущество перед знаковым состоит в том, что в рамках одной 8-битной системы мы можем получить любое число от 0 до 255.
Пока нам нужно складывать или умножать положительные числа, беззнаковой записи достаточно. Но, как правило, более практичным решением является работа и с отрицательными числами. Полезная особенность представления дополнения до 2 состоит в том, что вычитание эквивалентно сложению отрицательного числа, с которым мы можем справиться.
Измерение скорости реакции Практическая работа и решения.
Презентация на тему: «Измерение скорости реакции, практическая работа и решения.»- стенограмма презентации:
1 Измерение скорости реакции Практическая работа и решения
2 Главное меню Метод 1: Сбор газа 4. Вычислите изменение объема газа в течение первой, второй и третьей третей времени.Δ объем газа = разница в объеме на каждую треть. 5. Вычислите изменение количества молей газа в течение каждой трети реакции, затем разделите полученное значение на объем раствора (в дм 3), чтобы получить изменение концентрации. n = v / M v c = n / v (считайте значения с вашего графика) 6. Используйте уравнение во введении, чтобы рассчитать скорость реакции в течение каждой трети эксперимента. Скорость (плесень -3 с -1) = Δ [продукты] / Δ время 7. Как сравниваются три скорости? Попробуй объяснить разницу? Скорость должна быть выше вначале, потому что концентрация реагентов самая высокая.Больше сталкивающихся частиц реагента, более высокая частота столкновений, увеличенное количество успешных столкновений обеспечивает более высокую скорость превращения в продукты. (сек) Анализ: 1. Напишите сбалансированное уравнение реакции. Na 2 (CO 3) + 2HCl 2NaCl + CO 2 + H 2 O 2. Постройте график зависимости объема собранного газа от времени с линией (изогнутой) наилучшего соответствия. 3 Используйте вашу линейку, которая лучше всего подходит для определения объема газа, собранного на одну треть, две трети и на всем протяжении реакции.
3 Метод 2 из главного меню: Анализ метода йодных часов: 1.Рассчитайте количество молей тиосульфата натрия, участвующих в реакции. n = n / M r = 9,5 / 248,2 = 0,0383 моль тиосульфата натрия 2. Рассчитайте концентрацию тиосульфата натрия в растворе A c = n / v = 0,0383 / 0,02 = 1,92 молд · м -3 3. Используйте уравнения реакции для определения количество молей йода, образовавшееся в момент изменения цвета. S 2 O 3 2-: I 2 2: 1 соотношение из уравнения Число молей I 2 = 0,0192 4. Определите изменение концентрации I 2 (при условии, что часы его не съели).Когда йод образуется при изменении цвета c = n / v = 0,0192 / 0,04 = 0,479 м3 -3 5. Рассчитайте скорость реакции. Скорость реакции = Δ [I 2] / Δ t = (0,479 — 0) / Δ t (подставьте, сколько времени потребовалось для изменения цвета в секундах)
4 Анализ главного меню: 1. Напишите сбалансированное уравнение для этой реакции… исследуйте его, если нужно. Na 2 S 2 O 3 + 2HCl 2NaCl + SO 2 + S + H 2 O 2. Определите скорость реакции (Примечание: «концентрация» серы, необходимая для затемнения пятна, составляет около 7.5 х 10 -3 моль дм -3). Скорость реакции = Δ [S] / Δ t = (7,5 x 10-3 — 0) / Δ t 3. Вычислите относительную неопределенность скорости, которую вы только что определили. В частности, вам нужно будет подумать о том, насколько точно вы выберете время. Относительная погрешность секундомера = (0,1 / Δ t) x 100 Относительная погрешность (2) измерительного цилиндра = (0,25 / 10) x 100 x 2 = 5% Сложите относительные погрешности вместе Метод 3: Метод скрытых меток
Подготовка к практическому экзамену по химии
Практический экзамен — это проверка того, способен ли студент применить теоретические знания в практической жизни.На практическом экзамене по химии вы должны проявлять особую осторожность при проведении эксперимента, так как при работе с кислотами вредно для здоровья. В этой статье я хотел бы описать, как подготовиться к практическому экзамену по химии.
Практический экзамен
Практический экзамен — это внедрение теоретических знаний в практическую работу. Благодаря практическому документу вы получили представление о том, как работать с соответствующей теорией и как она применяется в настоящей жизни.Практический экзамен оценивает ваши способности в практической работе . У вас очень хорошие практические навыки для получения хорошей работы. Потому что компаниям нужен был профессионал с хорошими практическими навыками. Как бы там ни было, совет по образованию включает практические предметы в курс, и это поможет вам познакомиться с инструментами и с тем, как с ними обращаться, а также с порядком работы каждого инструмента в различных областях. Сравнивать с теоретическим экзаменом практический экзамен довольно просто. Как бы там ни было, если мы получим ошибку во время экзамена, это вызовет стресс.Ошибка может быть вызвана вашей ошибкой или какой-либо внутренней или внешней ошибкой инструментов, которые используются в практическом экзамене. И у вас нет практики, как в теоретической работе, так как весь инструмент, используемый в практической работе, недоступен в вашем доме, как в школе или колледже. Так что вы должны подготовиться к экзамену с точки зрения начала практического занятия. Так как у вас не должно появиться много времени на доработку с проведением эксперимента.Вы можете изучать только процедуры, теорию и т. Д. Таким образом, вы должны хорошо понимать основы работы и обращения с инструментом или машиной во время самого занятия. Только тогда вы сможете хорошо сдать практический экзамен. Наибольшая оценка на практическом экзамене дает проведение эксперимента и получение результата. Практический экзамен состоит из следующей процедуры применения, проведения эксперимента, результатов, подведения итогов, вывода и viva.
Существуют разные практические экзамены по разным предметам, а также разные способы написания экзамена.Здесь я хочу рассказать о практическом экзамене по химии и о том, как пройти этот экзамен.
Практический экзамен по химии
Практический экзамен по химии — это время, когда студенты могут чувствовать себя очень трудными, поскольку любая небольшая ошибка может привести к ошибке в результате. Всегда проявляйте особую осторожность при проведении обследования. Вы должны досконально знать концепцию каждого эксперимента, только тогда вы сможете предсказать результат. вы должны начинать подготовку с того момента, когда вы проводите эксперимент во время эксперимента, при проведении эксперимента необходимо соблюдать осторожность, поскольку он может привести к несчастному случаю из-за использования высококонцентрированных химикатов.
Шаги для сдачи практического экзамена по химии:
1. Вы задали вопрос, внимательно прочитаете его и полностью поймете вопрос, после чего только вы сможете решить, какой эксперимент выбрать для экзамена. Если вы знаете концепцию проведения каждого эксперимента во время урока, это совсем не сложная задача. Но вы должны тщательно продумывать идеи каждого эксперимента. И найдите цель и проделайте после этого следующую процедуру.
2.После того, как вы нашли и записали цель эксперимента, следующая задача — узнать принцип конкретного эксперимента. Здесь вы должны знать основное уравнение и теорию по теме. Только тогда вы сможете понять, достигли ли мы результата.
3. Следующим шагом является выполнение процедуры эксперимента. У разных экспериментов разные процедуры. Таким образом, вы должны знать, как провести конкретный эксперимент, и вы должны знать, что необходимо для проведения эксперимента. Выполняя процедуру, вы должны провести эксперимент.Это основа эксперимента, которую следует тщательно проводить во время практического занятия. Только тогда вы сможете вспомнить, что делать во время его выполнения. Вы должны проявлять особую осторожность при проведении эксперимента, поскольку вероятность аварии выше, поскольку мы используем химические вещества, такие как высококонцентрированные кислоты. И вам следует проявлять особую осторожность при приеме химикатов, постарайтесь взять точное количество для проведения эксперимента, только тогда вы сможете получить фактический результат. И вам следует ознакомиться с каждым инструментом, с которым вы работаете во время эксперимента.И это может быть стекло, поэтому с этим оборудованием следует быть очень осторожным. Для оценочного эксперимента вы должны провести взвешивание материала, стандартизацию материала, а затем оценку.
4. Следующим шагом является наблюдение и запись эксперимента, который мы проводим. Здесь мы должны предоставить столбцы табуляции для ввода значения наблюдения. Следует проявлять осторожность, когда мы наблюдаем значение. Ошибка в наблюдении может также привести к ошибке в результате и потере вашей оценки.Так что будьте особенно осторожны и внимательны, принимая значение и записывая его. И не забывайте каждый раз вводить значение. Поскольку повторно ввести значение непросто из-за изменения статуса химикатов, для повторного ввода мы должны повторить процедуру, и это займет много времени. Поэтому всегда делайте правильные и точные показания, снимая наблюдение .
5. Следующий шаг — расчет. Здесь вы выполняете расчет с наблюдаемым значением. И вы должны знать основное уравнение для выполнения расчета.Только тогда вы сможете произвести расчет по эксперименту. И после расчета нужно сделать результат. Результат должен содержать то, с какой целью вы проводили эксперимент. Если необходимо, предоставьте график.
Глава 7 — Растворы — Химия
Глава 7: Растворы A Стехиометрия раствора
7.1 Введение
7.2 Типы решений
7.3 Растворимость
7,4 Температура и растворимость
7.5 Влияние давления на растворимость газов: закон Генри
7,6 Твердые гидраты
7.7 Концентрация раствора
7.7.1 Молярность
7.7.2 Количество частей на решения
7,8 Разведения
7,9 Концентрации ионов в растворе
7.10 Внимание к окружающей среде: загрязнение свинцом
7.11 Резюме
7.12 Ссылки
7.1 Введение:
Напомним из Главы 1, что растворы определены как гомогенные смеси, которые перемешаны настолько тщательно, что ни один компонент не может наблюдаться независимо от другого. Решения повсюду вокруг нас. Например, воздух — это решение. Если вы живете рядом с озером, рекой или океаном, этот водоем — не чистый H 2 O, но, скорее всего, решение.Многие из того, что мы пьем, например газированные напитки, кофе, чай и молоко, являются растворами. Решения — большая часть повседневной жизни. Многие химические процессы, происходящие вокруг нас, происходят в растворе. Фактически, большая часть химии, которая происходит в нашем собственном организме, происходит в растворах, и многие растворы, такие как раствор лактата Рингера для внутривенного введения, важны для здравоохранения. В нашем понимании химии нам нужно немного разбираться в растворах. В этой главе вы узнаете об особых характеристиках решений, их характеристиках и некоторых их свойствах.
Навыки для развития
- Определите эти термины: раствор, растворенное вещество и растворитель.
- Различают растворы, смеси и коллоиды.
- Опишите различные типы решений.
- Различают ненасыщенные, насыщенные и перенасыщенные растворы.
Главный компонент раствора называется растворитель , а второстепенный компонент (ы) называется растворенным веществом . Если оба компонента в растворе составляют 50%, термин «растворенное вещество» может относиться к любому компоненту.Когда газообразный или твердый материал растворяется в жидкости, газ или твердый материал называется растворенным веществом. Когда две жидкости растворяются друг в друге, основной компонент называется растворителем , а второстепенный компонент — растворенным веществом .
Многие химические реакции протекают в растворах, и растворы также тесно связаны с нашей повседневной жизнью. Воздух, которым мы дышим, жидкости, которые мы пьем, и жидкости в нашем теле — все это решения.Кроме того, нас окружают такие решения, как воздух и вода (в реках, озерах и океанах).
По теме решений мы включаем следующие разделы.
- Типы растворов: газообразные, жидкие и твердые растворы в зависимости от состояния раствора.
- Стехиометрия раствора: выражение концентрации в различных единицах (масса на единицу объема, моль на единицу объема, процент и доли), расчеты стехиометрии реакции с использованием растворов.
- Растворы электролитов: растворы кислот, оснований и солей, в которых растворенные вещества диссоциируют на положительные и отрицательные гидратированные ионы.
- Метатезис или обменные реакции: реакция электролитов, приводящая к нейтральным молекулам, газам и твердым веществам.
Решение проблем стехиометрии раствора требует концепций, представленных в стехиометрии в главе 6, которая также обеспечивает основу для обсуждения реакций.
(Вернуться к началу)
7.2 типа решений
В главе 1 вы познакомились с концепцией смеси , которая представляет собой вещество, состоящее из двух или более веществ. Напомним, что смеси могут быть двух типов: гомогенные и гетерогенные, где гомогенные смеси сочетаются настолько тесно, что их можно рассматривать как единое вещество, хотя это не так. Гетерогенные смеси, с другой стороны, неоднородны и имеют участки смеси, которые выглядят иначе, чем другие участки смеси.Гомогенные смеси можно разделить на две категории: коллоиды и растворы. Коллоид — это смесь, содержащая частицы диаметром от 2 до 500 нм. Коллоиды кажутся однородными по своей природе и имеют одинаковый состав, но являются мутными или непрозрачными. Молоко — хороший пример коллоида. Истинные растворы имеют размер частиц типичного иона или небольшой молекулы (от 0,1 до 2 нм в диаметре) и прозрачны, хотя могут быть окрашены. В этой главе основное внимание будет уделено характеристикам истинных решений.
Материал существует в трех состояниях: твердом, жидком и газообразном. Решения также существуют во всех этих состояниях:
- Газовые смеси обычно однородны и обычно представляют собой газо-газовые растворы . Для количественной обработки такого типа растворов выделим единицу газам. Атмосфера представляет собой газообразный раствор, состоящий из азота, кислорода, аргона, двуокиси углерода, воды, метана и некоторых других второстепенных компонентов. Некоторые из этих компонентов, такие как вода, кислород и углекислый газ, могут различаться по концентрации в разных местах на Земле в зависимости от таких факторов, как температура и высота над уровнем моря.
- Когда молекулы газа, твердого вещества или жидкости диспергированы и смешаны с молекулами жидкости, гомогенные (однородные) состояния называются жидкими растворами . Твердые вещества, жидкости и газы растворяются в жидком растворителе с образованием жидких растворов. В этой главе большая часть химии, которую мы обсудим, происходит в жидких растворах, где вода является растворителем.
- Многие сплавы, керамика и полимерные смеси — это твердые растворы . В определенном диапазоне медь и цинк растворяются друг в друге и затвердевают с образованием твердых растворов, называемых латунью.Серебро, золото и медь образуют множество различных сплавов с уникальным цветом и внешним видом. Сплавы и другие твердые растворы важны в мире химии материалов.
(Вернуться к началу)
7.3 Растворимость
Максимальное количество вещества, которое может быть растворено в данном объеме растворителя, называется растворимостью . Часто растворимость в воде выражается в граммах / 100 мл. Раствор, не достигший максимальной растворимости, называется ненасыщенным раствором . Это означает, что к растворителю все еще может быть добавлено больше растворенного вещества, и растворение все равно будет происходить.
Раствор, достигший максимальной растворимости, называется насыщенным раствором . Если в этот момент добавить больше растворенного вещества, оно не растворится в растворе. Вместо этого он останется в осадке в виде твердого вещества на дне раствора. Таким образом, часто можно сказать, что раствор является насыщенным, если присутствует дополнительное растворенное вещество (оно может существовать в виде другой фазы, такой как газ, жидкость или твердое вещество).В насыщенном растворе нет чистого изменения количества растворенного вещества, но система никоим образом не статична. Фактически растворенное вещество постоянно растворяется и откладывается с одинаковой скоростью. Такое явление называется равновесие . Например:
В особых случаях раствор может быть перенасыщенным . Перенасыщенные растворы — это растворы, в которых растворенные вещества растворяются за пределами нормальной точки насыщения.Обычно для создания перенасыщенного раствора требуются такие условия, как повышенная температура или давление. Например, ацетат натрия имеет очень высокую растворимость при 270 К. При охлаждении такой раствор остается растворенным в так называемом метастабильном состоянии . Однако, когда в раствор добавляется кристалл затравки , дополнительное растворенное вещество быстро затвердевает. В процессе кристаллизации выделяется тепло, и раствор становится теплым. Обычные грелки для рук используют этот химический процесс для выработки тепла.
Видео 7.1: Видео, показывающее кристаллизацию перенасыщенного раствора ацетата натрия. Видео: Школа естественных и математических наук Северной Каролины
Итак, как мы можем предсказать растворимость вещества?
Одна полезная классификация материалов — полярность. Читая о ковалентных и ионных соединениях в главах 3 и 4, вы узнали, что ионные соединения имеют самую высокую полярность, образуя полные катионы и анионы внутри каждой молекулы, когда электроны передаются от одного атома к другому.Вы также узнали, что ковалентные связи могут быть полярными или неполярными по природе в зависимости от того, разделяют ли атомы, участвующие в связи, электроны неравномерно или поровну, соответственно. Напомним, что по разнице электроотрицательностей можно определить полярность вещества. Обычно ионная связь имеет разность электроотрицательностей 1,8 или выше, тогда как полярная ковалентная связь составляет от 0,4 до 1,8, а неполярная ковалентная связь составляет 0,4 или ниже.
Рисунок 7.1 Диаграмма разности электроотрицательностей. Приведенная выше диаграмма представляет собой руководство для определения типа связи между двумя разными атомами. Взяв разницу между значениями электроотрицательности для каждого из атомов, участвующих в связи, можно предсказать тип связи и полярность. Обратите внимание, что полный ионный характер достигается редко, однако, когда металлы и неметаллы образуют связи, они называются в соответствии с правилами ионного связывания.
Вещества с нулевой или низкой разностью электроотрицательности, такие как H 2 , O 2 , N 2 , CH 4 , CCl 4 , являются неполярными соединениями , тогда как H 2 O, NH 3 , CH 3 OH, NO, CO, HCl, H 2 S, PH 3 выше разность электроотрицательностей полярных соединений .Обычно соединения, имеющие сходную полярность, растворимы друг в друге. Это можно описать правилом:
Подобно Растворяется Нравится.
Это означает, что вещества должны иметь одинаковые межмолекулярные силы для образования растворов. Когда растворимое растворенное вещество вводится в растворитель, частицы растворенного вещества могут взаимодействовать с частицами растворителя. В случае твердого или жидкого растворенного вещества взаимодействия между частицами растворенного вещества и частицами растворителя настолько сильны, что отдельные частицы растворенного вещества отделяются друг от друга и, окруженные молекулами растворителя, входят в раствор.(Газообразные растворенные вещества уже имеют свои составляющие частицы, но концепция окружения частицами растворителя все еще применима.) Этот процесс называется solvatio n и проиллюстрирован на рисунке 7.2. Когда растворителем является вода, вместо сольватации используется слово гидратация .
Обычно полярные растворители растворяют полярные растворенные вещества, тогда как неполярные растворители растворяют неполярные растворенные вещества. В целом процесс растворения зависит от силы притяжения между частицами растворенного вещества и частицами растворителя.Например, вода представляет собой высокополярный растворитель, способный растворять многие ионные соли. На рис. 7.2 показан процесс растворения, в котором вода действует как растворитель для растворения кристаллической соли хлорида натрия (NaCl). Обратите внимание, что когда ионные соединения растворяются в растворителе, они распадаются на свободно плавающие ионы в растворе. Это позволяет соединению взаимодействовать с растворителем. В случае растворения хлорида натрия в воде ион натрия притягивается к частичному отрицательному заряду атома кислорода в молекуле воды, тогда как ион хлорида притягивается к частичным положительным атомам водорода.
Рисунок 7.2: Процесс растворения. Когда ионная соль, такая как хлорид натрия, показанная на (A), вступает в контакт с водой, молекулы воды диссоциируют ионные молекулы хлорида натрия в их ионное состояние, что показано в виде молекулярной модели на (B) твердого вещества. кристаллическая решетка хлорида натрия и (C) хлорид натрия, растворенный в водном растворителе. (Фотография хлорида натрия предоставлена Крисом 73).
Многие ионные соединения растворимы в воде, однако не все ионные соединения растворимы.Ионные соединения, растворимые в воде, существуют в растворе в ионном состоянии. На рис. 7.2 вы заметите, что хлорид натрия распадается на ион натрия и ион хлорида, когда он растворяется и взаимодействует с молекулами воды. В случае ионных соединений, которые не растворимы в воде, ионы настолько сильно притягиваются друг к другу, что не могут быть разделены частичными зарядами молекул воды. Следующая таблица может помочь вам предсказать, какие ионные соединения будут растворимы в воде.
Таблица 7.1 Правила растворимости
Диссоциация растворимых ионных соединений придает растворам этих соединений интересное свойство: они проводят электричество. Из-за этого свойства растворимые ионные соединения упоминаются как электролиты . Многие ионные соединения полностью диссоциируют и поэтому называются сильными электролитами . Хлорид натрия — пример сильного электролита.Некоторые соединения растворяются, но диссоциируют только частично, и растворы таких растворенных веществ могут лишь слабо проводить электричество. Эти растворенные вещества называются слабыми электролитами . Уксусная кислота (CH 3 COOH), входящее в состав уксуса, является слабым электролитом. Растворенные вещества, которые растворяются в отдельные нейтральные молекулы без диссоциации, не придают своим растворам дополнительную электропроводность и называются неэлектролитами . Полярные ковалентные соединения, такие как столовый сахар (C 12 H 22 O 11 ), являются хорошими примерами неэлектролитов .
Термин электролит используется в медицине для обозначения любых важных ионов, растворенных в водном растворе в организме. Важные физиологические электролиты включают Na + , K + , Ca 2 + , Mg 2 + и Cl — . Спортивные напитки, такие как Gatoraid, содержат комбинации этих ключевых электролитов, которые помогают восполнить потерю электролитов после тяжелой тренировки.
Точно так же решения могут быть получены путем смешивания двух совместимых жидкостей.Жидкость с более низкой концентрацией называется растворенным веществом , , а жидкость с более высокой концентрацией — растворителем . Например, зерновой спирт (CH 3 CH 2 OH) представляет собой полярную ковалентную молекулу, которая может смешиваться с водой. Когда два одинаковых раствора помещаются вместе и могут смешиваться в раствор, они считаются смешиваемыми . С другой стороны, жидкости, которые не имеют одинаковых характеристик и не могут смешиваться вместе, называются несмешивающимися .Например, масла, содержащиеся в оливковом масле, такие как олеиновая кислота (C 18 H 34 O 2 ), имеют в основном неполярные ковалентные связи, которые не обладают межмолекулярными силами, достаточно сильными, чтобы разорвать водородную связь между молекулы воды. Таким образом, вода и масло не смешиваются и считаются несмешивающимися .
Другие факторы, такие как температура и давление, также влияют на растворимость растворителя. Таким образом, при определении растворимости следует также учитывать эти другие факторы.
(Вернуться к началу)
7,4 Температура и растворимость
При рассмотрении растворимости твердых веществ соотношение температуры и растворимости не является простым или предсказуемым. На рис. 7.3 показаны графики зависимости растворимости некоторых органических и неорганических соединений в воде от температуры. Хотя растворимость твердого вещества обычно увеличивается с повышением температуры, нет простой взаимосвязи между структурой вещества и температурной зависимостью его растворимости.Многие соединения (например, глюкоза и CH 3 CO 2 Na) демонстрируют резкое увеличение растворимости с повышением температуры. Другие (такие как NaCl и K 2 SO 4 ) мало изменяются, а третьи (такие как Li 2 SO 4 ) становятся менее растворимыми с повышением температуры.
Рис. 7.3. Растворимость некоторых неорганических и органических твердых веществ в воде в зависимости от температуры. Растворимость может увеличиваться или уменьшаться с температурой; Величина этой температурной зависимости широко варьируется между соединениями.
Изменение растворимости в зависимости от температуры было измерено для широкого диапазона соединений, и результаты опубликованы во многих стандартных справочниках. Химики часто могут использовать эту информацию для разделения компонентов смеси с помощью фракционной кристаллизации , разделения соединений на основе их растворимости в данном растворителе. Например, если у нас есть смесь 150 г ацетата натрия (CH 3 CO 2 Na) и 50 г KBr, мы можем разделить два соединения, растворив смесь в 100 г воды при 80 ° C. а затем медленно охлаждают раствор до 0 ° C.Согласно температурным кривым на Рисунке 7.3 оба соединения растворяются в воде при 80 ° C, и все 50 г KBr остаются в растворе при 0 ° C. Однако только около 36 г CH 3 CO 2 Na растворимы в 100 г воды при 0 ° C, поэтому кристаллизуется примерно 114 г (150 г — 36 г) CH 3 CO 2 Na при охлаждении. Затем кристаллы можно отделить фильтрованием. Таким образом, фракционная кристаллизация позволяет нам восстановить около 75% исходного CH 3 CO 2 Na в практически чистой форме всего за одну стадию.
Фракционная кристаллизация — это распространенный метод очистки таких разнообразных соединений, как показано на рис. 7.3, и от антибиотиков до ферментов. Чтобы методика работала должным образом, интересующее соединение должно быть более растворимым при высокой температуре, чем при низкой, так что понижение температуры вызывает его кристаллизацию из раствора. Кроме того, примеси должны быть на более растворимы на , чем представляющее интерес соединение (как KBr в этом примере), и предпочтительно присутствовать в относительно небольших количествах.
Растворимость газов в жидкостях гораздо более предсказуема. Растворимость газов в жидкостях уменьшается с повышением температуры, как показано на рисунке 7.4. Привлекательные межмолекулярные взаимодействия в газовой фазе практически равны нулю для большинства веществ, потому что молекулы находятся так далеко друг от друга, когда находятся в газовой форме. Когда газ растворяется, это происходит потому, что его молекулы взаимодействуют с молекулами растворителя. Когда формируются эти новые силы притяжения, выделяется тепло. Таким образом, если к системе добавляется внешнее тепло, оно преодолевает силы притяжения между газом и молекулами растворителя и снижает растворимость газа.
Рис. 7.4 Зависимость растворимости нескольких обычных газов в воде от температуры при парциальном давлении 1 атм. Растворимость газов уменьшается с повышением температуры.
Уменьшение растворимости газов при более высоких температурах имеет как практические, так и экологические последствия. Любой, кто регулярно кипятит воду в чайнике или электрочайнике, знает, что внутри накапливается белый или серый налет, который в конечном итоге необходимо удалить.То же явление происходит в гораздо большем масштабе в гигантских котлах, используемых для подачи горячей воды или пара для промышленных применений, где это называется «котельная накипь», осадок, который может серьезно снизить пропускную способность труб горячего водоснабжения ( Рисунок 7.5). Проблема не только в современном мире: акведуки, построенные римлянами 2000 лет назад для транспортировки холодной воды из альпийских регионов в более теплые и засушливые регионы на юге Франции, были забиты аналогичными отложениями. Химический состав этих отложений умеренно сложен, но движущей силой является потеря растворенного диоксида углерода (CO 2 ) из раствора.Жесткая вода содержит растворенные ионы Ca 2+ и HCO 3 — (бикарбонат). Бикарбонат кальция [Ca (HCO 3 ) 2 ] довольно растворим в воде, но карбонат кальция (CaCO 3 ) совершенно нерастворим. Раствор бикарбонат-ионов может реагировать с образованием диоксида углерода, карбонат-иона и воды:
2HCO 3 — (вод.) → CO 2 2− (вод.) + H 2 O (л) + CO 2 (вод.)
Нагревание раствора снижает растворимость CO 2 , который уходит в газовую фазу над раствором.В присутствии ионов кальция ионы карбоната осаждаются в виде нерастворимого карбоната кальция, основного компонента котельной накипи.
Рисунок 7.5 Вес котла в водопроводе. Отложения карбоната кальция (CaCO 3 ) в трубах горячего водоснабжения могут значительно снизить пропускную способность труб. Эти отложения, называемые котельной накипью, образуются, когда растворенный CO 2 переходит в газовую фазу при высоких температурах.
В тепловое загрязнение , вода из озера или реки, которая используется для охлаждения промышленного реактора или электростанции, возвращается в окружающую среду при более высокой температуре, чем обычно.Из-за пониженной растворимости O 2 при более высоких температурах (рис. 7.4) более теплая вода содержит меньше растворенного кислорода, чем вода, когда она попадала в растение. Рыбы и другие водные организмы, которым для жизни необходим растворенный кислород, могут буквально задохнуться, если концентрация кислорода в их среде обитания будет слишком низкой. Поскольку теплая, обедненная кислородом вода менее плотна, она имеет тенденцию плавать на поверхности более холодной, плотной и более богатой кислородом воды в озере или реке, образуя барьер, препятствующий растворению атмосферного кислорода.В конце концов, если проблему не устранить, можно задохнуться даже в глубоких озерах. Кроме того, большинство рыб и других водных организмов, не являющихся млекопитающими, хладнокровны, а это означает, что температура их тела такая же, как температура окружающей среды. Температура, значительно превышающая нормальный диапазон, может привести к тяжелому стрессу или даже смерти. Системы охлаждения для электростанций и других объектов должны быть спроектированы таким образом, чтобы минимизировать любые неблагоприятные воздействия на температуру окружающих водоемов.На Тихоокеанском северо-западе популяции лососевых чрезвычайно чувствительны к изменениям температуры воды. Для этой популяции оптимальная температура воды составляет от 12,8 до 17,8 o C (55-65 o F). Помимо пониженного уровня кислорода, популяции лосося гораздо более восприимчивы к болезням, хищничеству и паразитарным инфекциям при более высоких температурах воды. Таким образом, тепловое загрязнение и глобальное изменение климата создают реальные проблемы для выживания и сохранения этих видов.Для получения дополнительной информации о влиянии повышения температуры на популяции лососевых посетите Focus Publication штата Вашингтон.
Аналогичный эффект наблюдается в повышении температуры водоемов, таких как Чесапикский залив, крупнейший эстуарий в Северной Америке, причиной которого является глобальное потепление. На каждые 1,5 ° C, которые нагревает вода в заливе, способность воды растворять кислород уменьшается примерно на 1,1%. Многие морские виды, находящиеся на южной границе своего распространения, сместили свои популяции дальше на север.В 2005 году угорь, который является важным местом обитания рыб и моллюсков, исчез на большей части залива после рекордно высоких температур воды. Предположительно, снижение уровня кислорода уменьшило популяцию моллюсков и других фильтрующих элементов, что затем уменьшило пропускание света, что позволило угрям расти. Сложные взаимоотношения в экосистемах, таких как Чесапикский залив, особенно чувствительны к колебаниям температуры, вызывающим ухудшение качества среды обитания.
(Вернуться к началу)
7.5 Влияние давления на растворимость газов: закон Генри
Внешнее давление очень мало влияет на растворимость жидкостей и твердых тел. Напротив, растворимость газов увеличивается с увеличением парциального давления газа над раствором. Эта точка проиллюстрирована на рисунке 7.6, где показано влияние повышенного давления на динамическое равновесие, которое устанавливается между молекулами растворенного газа в растворе и молекулами в газовой фазе над раствором.Поскольку концентрация молекул в газовой фазе увеличивается с увеличением давления, концентрация молекул растворенного газа в растворе в состоянии равновесия также выше при более высоких давлениях.
Рис. 7.6. Модель, показывающая, почему растворимость газа увеличивается при увеличении парциального давления при постоянной температуре. (a) Когда газ входит в контакт с чистой жидкостью, некоторые молекулы газа (пурпурные сферы) сталкиваются с поверхностью жидкости и растворяются.Когда концентрация растворенных молекул газа увеличилась так, что скорость, с которой молекулы газа уходят в газовую фазу, была такой же, как и скорость их растворения, было установлено динамическое равновесие, как показано здесь. (б) Увеличение давления газа увеличивает количество молекул газа в единице объема, что увеличивает скорость, с которой молекулы газа сталкиваются с поверхностью жидкости и растворяются. (c) По мере того как дополнительные молекулы газа растворяются при более высоком давлении, концентрация растворенного газа увеличивается до тех пор, пока не установится новое динамическое равновесие.
Взаимосвязь между давлением и растворимостью газа количественно описывается законом Генри, названным в честь его первооткрывателя, английского врача и химика Уильяма Генри (1775–1836):
C = кП
, где C — концентрация растворенного газа в состоянии равновесия, P — парциальное давление газа, а k — постоянная закона Генри , которая должна определяться экспериментально для каждой комбинации газа, растворителя, и температура.Хотя концентрация газа может быть выражена в любых удобных единицах, мы будем использовать исключительно молярность. Таким образом, единицами измерения постоянной закона Генри являются моль / (л · атм) = М / атм. Значения констант закона Генри для растворов нескольких газов в воде при 20 ° C приведены в таблице 7.2
Видеоурок по закону Генри от Академии Кана
Все материалы Khan Academy доступны бесплатно на сайте www.khanacademy.org
Как данные в таблице 7.2 демонстрируют, что концентрация растворенного газа в воде при заданном давлении сильно зависит от ее физических свойств. Для ряда родственных веществ дисперсионные силы Лондона увеличиваются с увеличением молекулярной массы. Таким образом, среди элементов группы 18 константы закона Генри плавно возрастают от He до Ne и до Ar. Из таблицы также видно, что O 2 почти в два раза растворимее, чем N 2 . Хотя силы лондонской дисперсии слишком слабы, чтобы объяснить такую большую разницу, O 2 является парамагнитным и, следовательно, более поляризуемым, чем N 2 , что объясняет его высокую растворимость.(Примечание: когда вещество парамагнитно , оно очень слабо притягивается полюсами магнита, но не сохраняет никакого постоянного магнетизма).
Таблица 7.2 Константы закона Генри для выбранных газов в воде при 20 ° C
Парциальное давление газа можно выразить как концентрацию, записав закон Генри как P газ = C / k. Это важно во многих сферах жизни, включая медицину, где обычно измеряются газы крови, такие как кислород и углекислый газ.Поскольку парциальное давление и концентрация прямо пропорциональны, если парциальное давление газа изменяется, а температура остается постоянной, новую концентрацию газа в жидкости можно легко рассчитать с помощью следующего уравнения:
Где C 1 и P 1 — соответственно концентрация и парциальное давление газа в исходном состоянии, а C 2 и P 2 — концентрация и парциальное давление, соответственно, газа в конечном состоянии.Например:
Практическая задача: Концентрация CO 2 в растворе составляет 0,032 М при 3,0 атм. Какова концентрация CO 2 при давлении 5,0 атм?
Решение: Чтобы решить эту проблему, сначала мы должны определить, что мы хотим найти. Это концентрация CO 2 при давлении 5,0 атм. Эти два значения представляют C 2 = ?? и P 2 = 5.0 атм. На этом этапе будет проще всего изменить приведенное выше уравнение, чтобы найти C 2 . Далее нам нужно определить начальные условия: C 1 = 0,032 M и P 1 = 3,0 атм. Затем мы можем подставить эти значения в уравнение и решить для C 2 :
Газы, которые химически реагируют с водой, такие как HCl и другие галогениды водорода, H 2 S и NH 3 , не подчиняются закону Генри; все эти газы гораздо более растворимы, чем предсказывает закон Генри.Например, HCl реагирует с водой с образованием H + (водн.) И Cl — (водн.), , а не растворенных молекул HCl, и его диссоциация на ионы приводит к гораздо более высокой растворимости, чем ожидалось для нейтральной молекулы. В целом газы, вступающие в реакцию с водой, не подчиняются закону Генри.
Обратите внимание на узор
Закон Генри имеет важные приложения. Например, пузырьки CO 2 образуются, как только открывается газированный напиток, потому что напиток был разлит под CO 2 при давлении более 1 атм.При открытии бутылки давление CO 2 над раствором быстро падает, и часть растворенного газа улетучивается из раствора в виде пузырьков. Закон Генри также объясняет, почему аквалангисты должны быть осторожны, чтобы медленно подняться на поверхность после погружения, если они дышат сжатым воздухом. При более высоком давлении под водой больше N 2 из воздуха растворяется во внутренних жидкостях дайвера. Если дайвер всплывает слишком быстро, быстрое изменение давления вызывает образование мелких пузырьков N 2 по всему телу, состояние, известное как «изгибы».«Эти пузырьки могут блокировать кровоток по мелким кровеносным сосудам, вызывая сильную боль и в некоторых случаях даже смертельный исход.
Из-за низкой константы закона Генри для O 2 в воде уровни растворенного кислорода в воде слишком низки для удовлетворения энергетических потребностей многоклеточных организмов, включая человека. Чтобы увеличить концентрацию O 2 во внутренних жидкостях, организмы синтезируют хорошо растворимые молекулы-носители, которые обратимо связывают O 2 . Например, красные кровяные тельца человека содержат белок, называемый гемоглобином, который специфически связывает O 2 и облегчает его транспортировку из легких в ткани, где он используется для окисления молекул пищи с целью получения энергии.Концентрация гемоглобина в нормальной крови составляет около 2,2 мМ, и каждая молекула гемоглобина может связывать четыре молекулы O 2 . Хотя концентрация растворенного O 2 в сыворотке крови при 37 ° C (нормальная температура тела) составляет всего 0,010 мМ, общая концентрация растворенного O 2 составляет 8,8 мМ, что почти в тысячу раз больше, чем было бы возможно без гемоглобина. Синтетические переносчики кислорода на основе фторированных алканов были разработаны для использования в качестве экстренной замены цельной крови.В отличие от донорской крови, эти «кровезаменители» не требуют охлаждения и имеют длительный срок хранения. Их очень высокие константы закона Генри для O 2 приводят к концентрации растворенного кислорода, сравнимой с таковой в нормальной крови.
(Вернуться к началу)
7,6 Твердые гидраты:
Некоторые ионные твердые вещества принимают небольшое количество молекул воды в свою кристаллическую решетку и остаются в твердом состоянии.Эти твердые вещества называются твердыми гидратами . Твердые гидраты содержат молекулы воды, объединенные в определенном соотношении в качестве неотъемлемой части кристалла, которые либо связаны с металлическим центром, либо кристаллизовались с комплексом металла. Также сообщается, что такие гидраты содержат кристаллизационную воду или гидратную воду .
Ярким примером является хлорид кобальта (II), который меняет цвет с синего на красный при гидратации и поэтому может использоваться в качестве индикатора воды.
Рис. 7.7: Хлорид кобальта как пример твердого гидрата. Безводный хлорид кобальта (вверху слева) и его структура кристаллической решетки (внизу слева) по сравнению с гексагидратом хлорида кобальта (вверху справа) и его кристаллическая решетка (внизу справа). Обратите внимание, что молекулы воды, показанные красным (кислород) и белым (водород), интегрированы в кристаллическую решетку хлорида кобальта (II), показанного синим (кобальт) и зеленым (хлорид), в зависимости от полярности. Частично отрицательные атомы кислорода притягиваются к положительно заряженному кобальту, тогда как частично положительные атомы водорода притягиваются к отрицательно заряженным ионам хлорида.Изображения предоставлены Wikipedia Commons (вверху слева и внизу слева), Benjah-bmm27 (вверху справа) и Smokefoot (внизу справа)
Обозначение, используемое для обозначения твердого гидрата: « гидратированное соединение ⋅ n H 2 O », где n — количество молекул воды на формульную единицу соли. n обычно является низким целым числом, хотя возможны и дробные значения. Например, в моногидрате n равно единице, а в гексагидрате n равно 6.В примере на рис. 7.7 гидратированный хлорид кобальта будет обозначен: «хлорид кобальта (II) 6 H 2 O». Числовые префиксы греческого происхождения, которые используются для обозначения твердых гидратов:
- Hemi — 1/2
- моно — 1
- Sesqui — 1½
- Di — 2
- Три — 3
- Тетра — 4
- Пента — 5
- Hexa — 6
- Hepta — 7
- Окта — 8
- Нона — 9
- Дека — 10
- Undeca — 11
- Додека — 12
Гидрат, потерявший воду, называют ангидридом ; оставшуюся воду, если она есть, можно удалить только при очень сильном нагревании.Вещество, не содержащее воды, обозначается как безводное . Некоторые безводные соединения настолько легко гидратируются, что вытягивают воду из атмосферы и становятся гидратированными. Утверждается, что эти вещества гигроскопичны, и могут использоваться как осушители или осушители .
(Вернуться к началу)
7.7 Концентрация раствора
В химии концентрация определяется как содержание компонента, деленное на общий объем смеси.Все мы качественно представляем, что подразумевается под концентрацией . Любой, кто варил растворимый кофе или лимонад, знает, что слишком много порошка дает сильно ароматный и высококонцентрированный напиток, тогда как слишком мало приводит к разбавленному раствору, который трудно отличить от воды. Количественно концентрация раствора описывает количество растворенного вещества, которое содержится в определенном количестве этого раствора. Знание концентрации растворенных веществ важно для контроля стехиометрии реагентов для реакций, протекающих в растворе, и имеет решающее значение для многих аспектов нашей жизни, от измерения правильной дозы лекарства до обнаружения химических загрязнителей, таких как свинец и мышьяк.Химики используют множество различных способов определения концентраций. В этом разделе мы рассмотрим наиболее распространенные способы представления концентрации раствора. К ним относятся: молярность и количество частей на раствор.
7.7.1 Молярность
Наиболее распространенной единицей концентрации является молярность , что также является наиболее полезным для расчетов, включающих стехиометрию реакций в растворе. Молярность (M) раствора — это количество молей растворенного вещества, присутствующего точно в 1 л раствора.
Таким образом, единицами молярности являются моль на литр раствора (моль / л), сокращенно M. Обратите внимание, что указанный объем является общим объемом раствора и включает как растворенное вещество, так и растворитель. Например, водный раствор, содержащий 1 моль (342 г) сахарозы в достаточном количестве воды, чтобы получить конечный объем 1,00 л, имеет концентрацию сахарозы 1,00 моль / л или 1,00 М. В химической записи квадратные скобки вокруг названия или формула растворенного вещества представляет собой концентрацию растворенного вещества.Итак
[сахароза] = 1,00 M
читается как «концентрация сахарозы 1,00 молярная». Приведенное выше уравнение можно использовать для расчета количества растворенного вещества, необходимого для получения любого количества желаемого раствора.
Пример проблемы:
Рассчитайте количество молей гидроксида натрия (NaOH), необходимое для получения 2,50 л 0,100 M NaOH.
Дано: (1) идентичность растворенного вещества = NaOH, (2) объем = 2,50 л и (3) молярность раствора = 0.100 моль / л (Примечание: при вычислении задач всегда записывайте единицы молярности как моль / л, а не М. Это позволит вам отменить единицы при выполнении расчета.)
Запрошено: количество растворенного вещества в молях
Стратегия: (1) Измените приведенное выше уравнение, чтобы найти желаемую единицу, в данном случае молей. (2) Еще раз проверьте все единицы в уравнении и убедитесь, что они совпадают. Выполните все необходимые преобразования, чтобы единицы совпадали. (3) Введите значения соответствующим образом и выполните математические вычисления.
Решение:
(1) Перепишите приведенное выше уравнение, чтобы найти количество молей.
(2) Еще раз проверьте все единицы в уравнении и убедитесь, что они совпадают.
Приведенные значения для этого уравнения: объем 2,50 л и молярность 0,100 моль / л. Единицы объема для обоих этих чисел указаны в литрах (L) и, следовательно, совпадают. Следовательно, никаких преобразований производить не нужно.
(3) Введите значения соответствующим образом и выполните математические вычисления.
Приготовление растворов
Обратите внимание, что в приведенном выше примере у нас все еще недостаточно информации, чтобы фактически приготовить раствор в лаборатории. Не существует оборудования, которое могло бы измерить количество молей вещества. Для этого нам нужно преобразовать количество молей образца в количество граммов, представленное этим числом. Затем мы можем легко использовать весы для взвешивания количества вещества, необходимого для приготовления раствора.Для примера выше:
Чтобы фактически приготовить раствор, обычно растворяют растворенное вещество в небольшом количестве растворителя, а затем, когда растворенное вещество растворяется, конечный объем может быть увеличен до 2,50 л. Если вы добавляете 10 г NaOH напрямую до 2,50 л конечный объем будет больше 2,50 л, а концентрация раствора будет меньше 0,100 М. Помните, что конечный объем должен включать как растворенное вещество, так и растворитель.
Рисунок 7.8 иллюстрирует процедуру приготовления раствора дигидрата хлорида кобальта (II) в этаноле.Обратите внимание, что объем растворителя не указан. Поскольку растворенное вещество занимает пространство в растворе, необходимый объем растворителя на меньше , чем желаемый общий объем раствора.
Рис. 7.8: Приготовление раствора известной концентрации с использованием твердого вещества. Чтобы приготовить раствор, сначала добавьте в колбу часть растворителя. Затем взвесьте необходимое количество растворенного вещества и медленно добавьте его к растворителю.После растворения в растворителе объем раствора можно довести до конечного объема раствора. Для показанной мерной колбы это обозначено черной линией на горловине колбы. В данном случае это 500 мл раствора. Мерные колбы бывают разных размеров, чтобы вместить разные объемы раствора. Градуированные цилиндры также можно использовать для точного доведения раствора до конечного объема. Другая стеклянная посуда, включая химические стаканы и колбы Эрленмейера, недостаточно точна для большинства решений.
Пример расчета молярности
Раствор на рисунке 7.8 содержит 10,0 г дигидрата хлорида кобальта (II), CoCl 2 · 2H 2 O, в этаноле, достаточном для приготовления ровно 500 мл раствора. Какова молярная концентрация CoCl 2 · 2H 2 O?
Дано: масса растворенного вещества и объем раствора
Запрошено: концентрация (M)
Стратегия:
1.Мы знаем, что молярность равна
моль / литр.2. Чтобы вычислить молярность, нам нужно выразить:
- масса в виде родинок
- объем в литрах
- Подставьте оба в уравнение выше и вычислите
Решение:
- Преобразование массы в моль. Мы можем использовать молярную массу для перевода граммов CoCl 2 · 2H 2 O в моль.
- Молярная масса CoCl 2 · 2H 2 O равна 165.87 г / моль (включая две молекулы воды, поскольку они являются частью структуры кристаллической решетки этого твердого гидрата!)
2. Перевести объем в литры
3. Подставьте значения в уравнение полярности:
7.7.2 Количество частей на решения
В потребительском и промышленном мире наиболее распространенный метод выражения концентрации основан на количестве растворенного вещества в фиксированном количестве раствора.Упомянутые здесь «количества» могут быть выражены в массе, в объеме или и в том, и в другом (т. Е. масса растворенного вещества в данном объеме раствора). Чтобы различать эти возможности, сокращения (m / м), (об / об) и (м / об).
В большинстве прикладных областей химии часто используется мера (м / м), тогда как в клинической химии обычно используется (м / об) с массой , выраженной в граммах, и объемом в мл.
Один из наиболее распространенных способов выражения таких концентраций как « частей на 100 », который мы все знаем как « процентов ».« Cent » — это префикс латинского происхождения, относящийся к числу 100
(L. centum ), как в столетии или столетии . Он также обозначает 1/100 (от L. centesimus ) как сантиметр и денежную единицу центов . Процентные растворы определяют количество растворенного вещества, которое растворено в количестве раствора, умноженное на 100. Процентные растворы могут быть выражены в единицах массы растворенного вещества на массу раствора (м / м%) или массы растворенного вещества на объем раствора (м / об.%) или объем растворенного вещества на объем раствора (об. / об.%).При создании процентного раствора важно указать, какие единицы измерения используются, чтобы другие также могли правильно принять решение. Также помните, что раствор — это сумма как растворителя, так и растворенного вещества, когда вы выполняете расчет процентов.
Раствор = Раствор + Растворитель
Таким образом, при вычислении процентных решений можно использовать следующее уравнение:
Пример 1:
В качестве примера, раствор этанола в воде с концентрацией 7,0% об. / Об. Должен содержать 7 мл этанола в общем количестве 100 мл раствора.Сколько воды в растворе?
В этой задаче мы знаем, что:
Раствор = Раствор + Растворитель
Таким образом, мы можем ввести значения, а затем решить неизвестное.
100 мл = 7 мл + X мл растворителя (в данном случае вода)
переместив 7 на другую сторону, мы видим, что:
100 мл — 7 мл = 93 мл H 2 O
Пример 2
Какое (м / об)% раствора, если 24.0 г сахарозы растворяется в общем растворе 243 мл?
Пример 3
Сколько граммов NaCl требуется для приготовления 625 мл 13,5% раствора?
Для более разбавленных растворов используются части на миллион (10 6 частей на миллион) и части на миллиард (10 9 ; частей на миллиард). Эти термины широко используются для обозначения количества следов загрязняющих веществ в окружающей среде.
Одинаковые процентные («части на сотню») единицы, ppm и ppb могут быть определены в единицах массы, объема или смешанных единиц массы-объема.Также существуют единицы ppm и ppb, определяемые по количеству атомов и молекул.
Массовые определения ppm и ppb приведены здесь:
Как ppm, так и ppb являются удобными единицами измерения концентраций загрязняющих веществ и других микропримесей в воде. Концентрации этих загрязнителей, как правило, очень низкие в очищенных и природных водах, и их уровни не могут превышать относительно низкие пороговые значения концентрации, не вызывая неблагоприятных последствий для здоровья и дикой природы.Например, EPA определило, что максимально безопасный уровень фторид-иона в водопроводной воде составляет 4 ppm. Встроенные фильтры для воды предназначены для снижения концентрации фторида и некоторых других незначительных примесей в водопроводной воде (рис. 7.9).
Рисунок 7.9. (a) В некоторых районах следовые концентрации загрязняющих веществ могут сделать нефильтрованную водопроводную воду небезопасной для питья и приготовления пищи. (b) Встроенные фильтры для воды снижают концентрацию растворенных веществ в водопроводной воде.(кредит А: модификация работы Дженн Дарфи; кредит б: модификация работы «Вастатепаркстафф» / Wikimedia commons
При сообщении о загрязнителях, таких как свинец, в питьевой воде, концентрации ppm и ppb часто указываются в смешанных единицах измерения массы / объема. Это может быть очень полезно, поскольку нам легче думать о воде с точки зрения ее объема, а не массы. Кроме того, плотность воды составляет 1,0 г / мл или 1,0 мг / 0,001 мл, что упрощает преобразование между двумя единицами измерения.Например, если мы обнаружим, что содержание свинца в воде составляет 4 ppm, это будет означать, что есть:
7,74 Эквиваленты
Концентрации ионных растворенных веществ иногда выражаются в единицах, называемых эквивалентами (уравнение). Один эквивалент равен 1 моль положительного или отрицательного заряда.

 | План-конспект урока по химии (9 класс) на тему:
| План-конспект урока по химии (9 класс) на тему:

 ).Вареные, затем охлажденные
).Вареные, затем охлажденные Формы осадка. Осадок растворяется
Формы осадка. Осадок растворяется
 Этот курс направлен на то, чтобы вооружить студентов рабочими знаниями и набором практических навыков для профессиональной аналитической химии и ее применения в ряде экологических систем и промышленных приложений. Студенты будут обучены методам, используемым профессиональными химиками для определения химического состава и анализа на следовые соединения, которые являются ключевыми для рассматриваемых экологических систем. Основы аналитической строгости будут рассмотрены и развиты как в теории, так и на практике.
Этот курс направлен на то, чтобы вооружить студентов рабочими знаниями и набором практических навыков для профессиональной аналитической химии и ее применения в ряде экологических систем и промышленных приложений. Студенты будут обучены методам, используемым профессиональными химиками для определения химического состава и анализа на следовые соединения, которые являются ключевыми для рассматриваемых экологических систем. Основы аналитической строгости будут рассмотрены и развиты как в теории, так и на практике. Ки (
Ки (
 , W.H. Фримен.
, W.H. Фримен.  adelaide.edu.au/mathslearning/
adelaide.edu.au/mathslearning/ Это включает в себя как формальное время контакта, необходимое для курса (например, лекции и практические занятия), так и время без контакта (например, чтение и повторение).
Это включает в себя как формальное время контакта, необходимое для курса (например, лекции и практические занятия), так и время без контакта (например, чтение и повторение).
 Остальные занятия позволят студентам реализовать эти навыки, подготовить стандарты и разработать аналитические методологии, качественно и количественно оценить результаты и поместить эти анализы в более широкий экологический контекст. Будет обеспечено обучение и руководство по распространению результатов этих расследований в различных форматах.
Остальные занятия позволят студентам реализовать эти навыки, подготовить стандарты и разработать аналитические методологии, качественно и количественно оценить результаты и поместить эти анализы в более широкий экологический контекст. Будет обеспечено обучение и руководство по распространению результатов этих расследований в различных форматах.
 Результаты обучения по этому курсу в значительной степени зависят от лабораторного опыта и практики. Таким образом, пропуск какого-либо практического занятия в семестре приведет к тому, что для курса будет выставлена оценка FAIL. Учащимся, не посещающим занятия по медицинским причинам или из соображений сострадания, будет предоставлена возможность восполнить пропущенные практические занятия.
Результаты обучения по этому курсу в значительной степени зависят от лабораторного опыта и практики. Таким образом, пропуск какого-либо практического занятия в семестре приведет к тому, что для курса будет выставлена оценка FAIL. Учащимся, не посещающим занятия по медицинским причинам или из соображений сострадания, будет предоставлена возможность восполнить пропущенные практические занятия. Студенты индивидуально оцениваются сотрудниками и их сверстниками.
Студенты индивидуально оцениваются сотрудниками и их сверстниками. У студентов будет множество возможностей продемонстрировать свои навыки в течение семестра. Студенты должны как можно скорее связаться с координатором курса, чтобы обсудить макияж.
У студентов будет множество возможностей продемонстрировать свои навыки в течение семестра. Студенты должны как можно скорее связаться с координатором курса, чтобы обсудить макияж. Студенты должны подать заявку на продление к Координатору курса до наступления срока выполнения задания.Продления не будут предоставлены из-за неправильного распределения времени. Бланк заявки на продление оценки можно получить по адресу: http://www.sciences.adelaide.edu.au/current/
Студенты должны подать заявку на продление к Координатору курса до наступления срока выполнения задания.Продления не будут предоставлены из-за неправильного распределения времени. Бланк заявки на продление оценки можно получить по адресу: http://www.sciences.adelaide.edu.au/current/