Базовый уровень ФГОС, Габриелян Олег Сергеевич , Просвещение/ Дрофа , 9785090881777 2022г. 1079,00р.
Габриелян Олег Сергеевич
1079,00р.
-20% после регистрации
В наличии в 4 магазинах
Иркутск, ПродаЛитЪ Иркутск-2
Иркутск, ПродаЛитЪ Мир книг
Саянск, ПродалитЪ Саянск
Тулун, Тулун ООО «Знание»
Цена в магазине может отличаться
от цены, указанной на сайте.
Поделиться ссылкой в:
Издательство:Просвещение/ Дрофа
Бренд:Дрофа
ISBN:978-5-09-088177-7
Штрих-код:9785090881777
Страниц:192
Тип обложки:Твердая
Год:2022
НДС:10%
Возраст:от 15 лет до 17 лет
Код:121019
Описание
Учебник продолжает курс химии, изложенный в учебниках «Химия. 8 класс» и «Химия. 9 класс» автора О. С. Габриеляна. Может быть использован при изучении курса органической химии на базовом уровне. Учебник соответствует Федеральному государственному образовательному стандарту среднего (полного) общего образования, одобрен РАО и РАН, включен в Федеральный перечень учебников.
8 класс» и «Химия. 9 класс» автора О. С. Габриеляна. Может быть использован при изучении курса органической химии на базовом уровне. Учебник соответствует Федеральному государственному образовательному стандарту среднего (полного) общего образования, одобрен РАО и РАН, включен в Федеральный перечень учебников.
Смотреть все
1079,00р.
-20% после регистрации
Химия. 11 класс: Базовый уровень: Учебник ФГОС (2022 г.)
Габриелян Олег Сергеевич
1079,00р.
-20% после регистрации
Химия. 10 класс: Учебник: Базовый уровень ФГОС (2022 г.)
Габриелян Олег Сергеевич
918,00р.
-20% после регистрации
Химия. 11 класс: Базовый уровень: Учебник ФГОС (2021 г.)
Габриелян Олег Сергеевич
969,00р.
-20% после регистрации
Химия. 7 класс: Вводный курс: Учебник ФГОС (2021 г.)
Габриелян Олег Сергеевич
1182,00р.
Химия. 8 класс: Учебное пособие (2022 г.)
Габриелян Олег Сергеевич
Магазины
777,50р.
Химия. 10 кл.: Учебник: Базовый уровень ФГОС (2021 г.)
Габриелян Олег Сергеевич
Магазины
269,00р.
Химия. 7 класс: Рабочая тетрадь к учеб. пособию Габриеляна О.С. (2021 г.)
Габриелян Олег Сергеевич
Магазины
744,00р.
Химия. 9 кл.: Учебное пособие (ФГОС) (2020 г.)
Габриелян Олег Сергеевич
Магазины
725,50р.
Химия. 11 кл.: Базовый уровень: Учебник ФГОС (2019 г.)
Габриелян Олег Сергеевич
Магазины
725,50р.
Химия. 10 кл.: Учебник: Базовый уровень ФГОС (2019 г.
 )
)Габриелян Олег Сергеевич
Магазины
194,88р.
Химия. 8-9 кл.: Задачи по химии и способы их решения (2018 г.)
Габриелян Олег Сергеевич
Магазины
812,70р.
Химия. 11 кл.: Учебник. Углубл. уровень ФГОС (2018 г.)
Габриелян Олег Сергеевич
Магазины
542,50р.
Химия. 7 кл.: Учеб. пособие (2017 г.)
Габриелян Олег Сергеевич
Магазины
212,80р.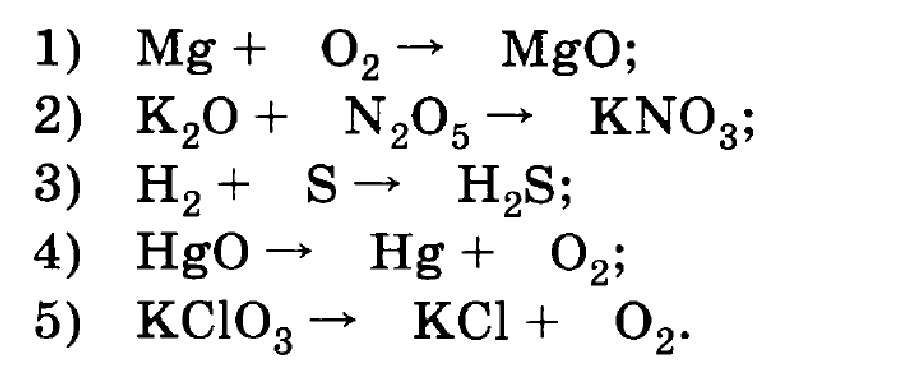
Химия. 7 кл.: Рабочая тетрадь к учеб. пос. Габриеляна О.С. ФГОС (2017 г.)
Габриелян Олег Сергеевич
Магазины
211,20р.
Химия. 9 кл.: Контрольные работы к учеб. Габриеляна ФГОС (2017 г.)
Габриелян Олег Сергеевич
Магазины
173,50р.
Химия. 11 кл.: Рабочая тетрадь. Базовый уровень ФГОС (2016 г.)
Габриелян Олег Сергеевич
Магазины
212,80р.
Химия. 7 кл.: Рабочая тетрадь к учеб. пос. Габриеляна О.
 С. ФГОС
(2016 г.)
С. ФГОС
(2016 г.)Габриелян Олег Сергеевич
Магазины
119,00р.
Химия. 10 кл.: Контрольные и проверочные работы. Базовый уров (2015 г.)
Габриелян Олег Сергеевич
Магазины
110,00р.
Химия. 8 кл.: Контрольные и проверочные работы ФГОС (2015 г.)
Габриелян Олег Сергеевич
Магазины
150,00р.
Химия. 7 кл.: Рабочая тетрадь к учеб. пос. Габриеляна О.С. ФГОС (2015 г.)
Габриелян Олег Сергеевич
Магазины
Смотреть все
1046,00р.
-20% после регистрации
Литература. 7 класс: Учебник: В 2 частях Часть 2 ФП (2022 г.)
Коровина В.Я.
1255,00р.
Технология. 8-9 классы: Учебник ФГОС (2022 г.)
Глозман Е.С., Кожина О.А., Хотунцев Ю.Л.
Магазины
912,00р.
Изобразительное искусство в театре, кино, на телевидении. 8 кл.: Учебник ФП (2020 г.)
Питерских А.С.
Магазины
1477,00р.
-20% после регистрации
Химия. 9 класс: Учебник: Неорганическая, органическая химия ФП (2022 г.
 )
)Рудзитис Г.Е.
974,50р.
-20% после регистрации
Химия. 7 класс: Учебник ФП (2022 г.)
Габриелян О.С., Остроумова И.Г., Сладков С.А.
786,00р.
ОБЖ. 11 класс: Учебное пособие: Базовый уровень ФП (2021 г.)
Марков В.В. Латчук В.Н. Миронов С.К.
Магазины
729,50р.
-20% после регистрации
Русский язык. 6 кл.: Учебник. В 2 ч. Ч.2 ФП (2021 г.)
Рыбченкова Л.М., Александрова О.М., Загорвоск
994,00р.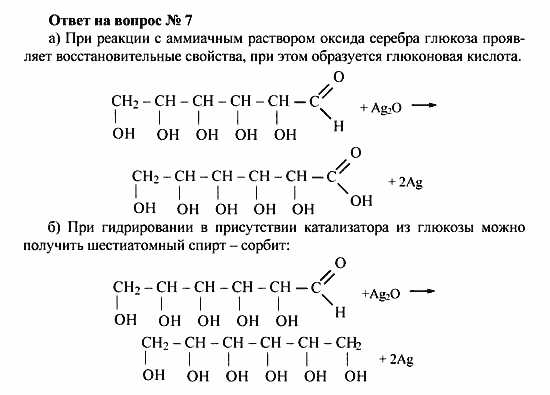
-20% после регистрации
Английский язык. 9 кл.: Учебник ФГОС (2020 г.)
Биболетова М.З.
1322,00р.
-20% после регистрации
Алгебра и начала математического анализа. 11 кл.: Учебник ФП (2021 г.)
Никольский С.М., Потапов М.К.
1028,00р.
Информатика. 11 кл.: Базовый уровень: Учебник ФГОС (2020 г.)
Босова Л.Л., Босова А.Ю.
Магазины
945,00р.
-20% после регистрации
Россия в мире. 10 кл.
 : Учебник: Базовый уровень ФГОС
(2020 г.)
: Учебник: Базовый уровень ФГОС
(2020 г.)Волобуев О.В., Клоков В.А., Пономарев М.В.
812,00р.
Русский язык. 10-11 кл.: Учебник. Базовый уровень ФП (2021 г.)
Рыбченкова Л.М.
Магазины
1496,00р.
Всеобщая история. 9 класс: История Нового времени: Учебник ФП (2022 г.)
Юдовская А.Я, Баранов П.А., Ванюшкина Л.М.
Магазины
990,50р.
-20% после регистрации
Литература. 11 класс: Учебник: Базовый и углубленный уровни ФГОС (2022 г.
 )
)Ланин Б.А., Устинова Л.Ю., Шамчикова В.М.
1009,00р.
Химия. 11 класс: Учебник. Базовый уровень (2021 г.)
Габриелян О.С., Остроумов И.Г., Сладков С.А.
Магазины
635,00р.
-20% после регистрации
Русский язык. 5 класс: Учебник: В 2 частях Часть 2 ФП (2022 г.)
Разумовская М.М., Львова С .И., Капинос В.И.
972,00р.
-20% после регистрации
Литература. 11 класс: Учебник: В 2 частях: Часть 2 Базовый уровень ФП (2021 г.)
Михайлов О. Н., Щайтанов И.О., Чалмаев В.А.; П
Н., Щайтанов И.О., Чалмаев В.А.; П
1357,00р.
-20% после регистрации
Информатика. 10 класс: Базовый уровень: Учебник ФГОС (2022 г.)
Босова Л.Л., Босова А.Ю.
827,50р.
География. 10 кл.: Учебник: Углубленный уровень ФГОС (2020 г.)
Домогацких Е.М., Алексеевский Н.И.
Магазины
1351,00р.
-20% после регистрации
Информатика. 11 класс: Учебник. Базовый и углубленный уровни: В 2 частях Часть 2 (2022 г.)
Поляков К.Ю., Еремин Е.А.
Химия 10 класс — СУНЦ МГУ
Курс состоит из следующих блоков:
1. Состав и строение органических веществ. Классы соединений. Изомерия и номенклатура. Определение состава органических веществ.
Состав и строение органических веществ. Классы соединений. Изомерия и номенклатура. Определение состава органических веществ.
2. Алканы. Радикальное замещение. Переработка нефти, газа, угля.
3. Непредельные соединения. Электрофильное присоединение. Алкены, алкины, диены. Полимеризация.
4. Ароматические соединения. Электрофильное замещение.
5. Галогенпроизводные и гидроксильные соединения. Спирты и фенолы.
6. Альдегиды и кетоны.
7. Карбоновые кислоты.
8. Углеводы.
9. Нитропроизводные. Амины.
10. Аминокислоты, белки. Гетероциклы. Нуклеиновые кислоты.
Программа по химии для учеников 10 класса Центра дистанционного обучения СУНЦ МГУ
(курсивом выделен дополнительный материал)
- Введение в органическую химию
Состав и строение органических веществ. Основные положения теории химического строения А.М.Бутлерова. Явление изомерии. Типы химических формул: простейшие, молекулярные, структурные, пространственные.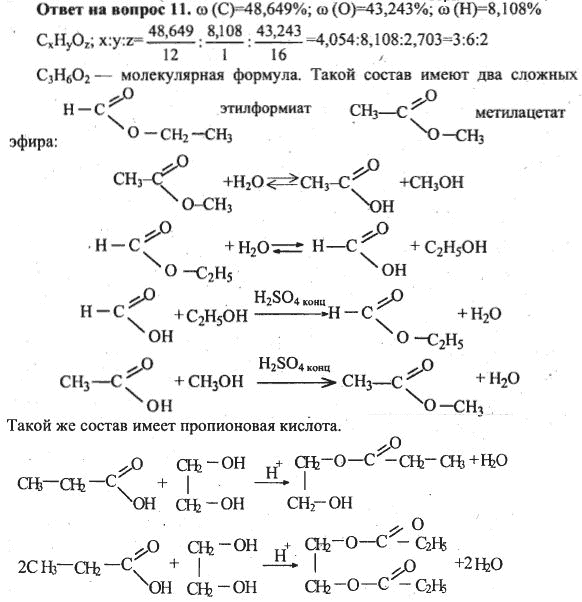
Ковалентная связь в органических соединениях. Энергия связи, полярность, направленность. Одинарные, двойные и тройные связи. Теория гибридизации. Геометрия простейших молекул.
Типы изомерии – структурной и пространственной. Понятие о взаимном влиянии атомов в молекулах. Индуктивный и мезомерный эффекты.
Классификация органических соединений. Основные признаки: скелет молекулы, степень ненасыщенности, наличие функциональных групп. Типы скелетов. Насыщенные и ненасыщенные соединения. Ациклические, алициклические и гетероциклические соединения. Важнейшие функциональные группы. Понятия: гомологи, гомологический ряд.
Основные положения современной международной номенклатуры органических веществ (JUPAC).
- Предельные углеводороды
Предельные углеводороды. Общая формула. Электронное и пространственное строение алканов. Номенклатура.
Физические и химические свойства алканов. Горение алканов. Реакции радикального замещения (галогенирование, нитрование).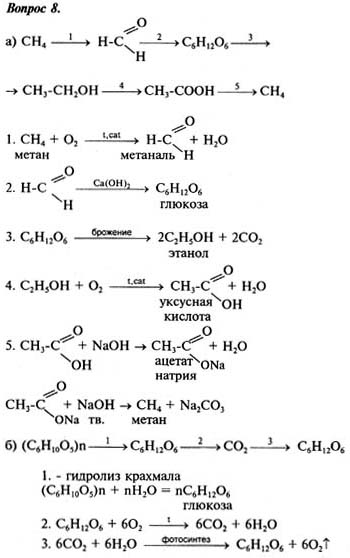 Механизм цепной радикальной реакции. Зависимость стабильности алкильных радикалов от их строения. Селективность в реакциях замещения первичных, вторичных и третичных атомов водорода в алканах. Дегидирование, дегидроциклизация, ароматизация и термическое разложение алканов. Конверсия метана.
Механизм цепной радикальной реакции. Зависимость стабильности алкильных радикалов от их строения. Селективность в реакциях замещения первичных, вторичных и третичных атомов водорода в алканах. Дегидирование, дегидроциклизация, ароматизация и термическое разложение алканов. Конверсия метана.
Понятие о циклоалканах. Строение циклоалканов, номенклатура, особенности малых циклов. Понятие о геометрической изомерии. Общая характеристика химических свойств, сравнение с алканами.
Природные источники углеводородов. Нефть и природный газ, попутный нефтяной газ. Каменный уголь. Состав нефти, основные классы входящих в нее углеводородов. Перегонка нефти. Основные виды нефтепродуктов.
Бензин. Понятие об октановом числе. Нефтепереработка.
Роль горючих ископаемых в жизни современного общества. Загрязнение окружающей среды продуктами горения углеводородов: глобальное увеличение концентрации углекислого газа в атмосфере, физиологическое действие оксида углерода (II), смог.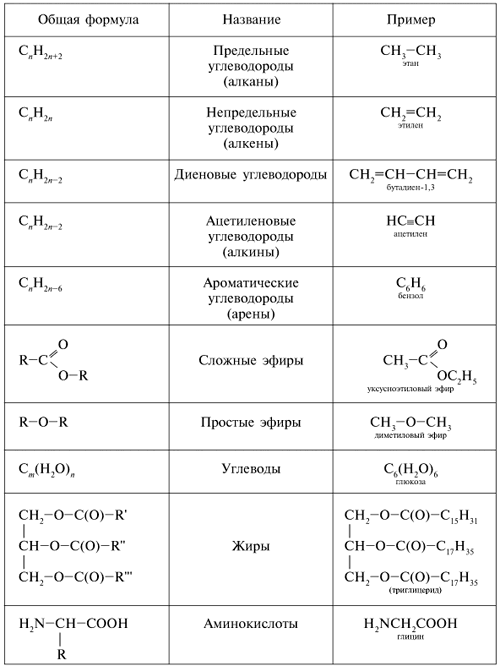
- Непредельные углеводороды
Алкены. Электронное и пространственное строение, номенклатура. Изомерия алкенов. Методы получения. Химические свойства алкенов: горение; присоединение водорода, галогенов, галогеноводородов, воды; окисление. С=С. Механизм реакций электрофильного присоединния — образование карбокатионов. Правило Марковникова. Реакции радикального присоединения. Различия в продуктах реакций пропена с бромоводородом по радикальному и ионному механизму. Аллильное хлорирование (бромирование). Качественные реакции.
Полимеризация. Понятия: полимер, мономер, концевые группы, средняя степень полимеризации, средняя молекулярная масса..Представление о радикальном и ионном (катионном и анионном) механизмах полимеризации. Атактические, изотактические и синдиотактические полимеры. Полимеризация по типу «голова к хвосту» и «голова к голове».
Полиэтилен, полипропилен, ПВХ, тефлон, полиакрилонитрил.
Алкины. Электронное и пространственное строение алкинов. Изомерия. Общая характеристика химических свойств алкинов. Сравнение с алкенами. Особенности реакций присоединения (гидрирование, галогенирование, гидрогалоненирование, гидратация — реакция Кучерова) и окисление. Сравнение с алкенами. Понятие о кислотности алкинов в ацетиленидах.
Изомерия. Общая характеристика химических свойств алкинов. Сравнение с алкенами. Особенности реакций присоединения (гидрирование, галогенирование, гидрогалоненирование, гидратация — реакция Кучерова) и окисление. Сравнение с алкенами. Понятие о кислотности алкинов в ацетиленидах.
Диеновые углеводороды. Сопряженные диены. Общая характеристика химических свойств, сравнение с алкенами. Реакции 1,2- и 1,4-присоединения. Каучук и гуттаперча, состав, строение. Вулканизация и синтез каучука.
Реакция Дильса-Альдера.
- Ароматические соединения
Ароматические углеводороды. Электронное и пространственное строение бензола. Понятие об ароматичности. Химические свойства бензола: реакции электрофильного замещения (бромирование, нитрование, алкилирование по Фриделю-Крафтсу) и радикального присоединения (реакции с водородом и хлором).
Производные бензола. Номенклатура. Взаимное влияние бензольного кольца и заместителей.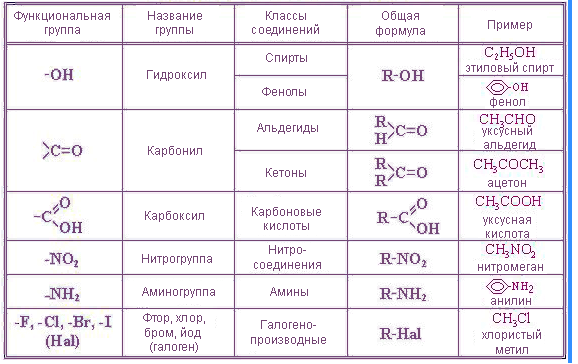 Направляющее влияние заместителей. Окисление аренов.
Направляющее влияние заместителей. Окисление аренов.
Понятие о полициклических аренах (нафталин, бензпирены)
- Галогенпроизводные и гидроксильные соединения. Спирты и фенолы
Галогенпроизводные углеводородов. Моно- и полигалогенпроизводные углеводородов, изомерия и номенклатура. Реакции нуклеофильного замещения. Представление о механизмах SN1 и SN2. Элиминирование. Правило Зайцева. Хлор- и фторсодержащие органические соединения, экологические проблемы, связанные с их применением. Галогенсодержащие пестициды.
Спирты. Одноатомные спирты. Электронное и пространственное строение. Изомерия. Номенклатура, физические свойства, роль водородных связей. Производство метанола и этанола.
Физиологическое действие спиртов.
Химические свойства: горение, окисление до альдегидов и карбоновых кислот, взаимодействие с щелочными металлами, галогеноводородами, дегидратация. Понятие о простых эфирах.
Понятие о многоатомных спиртах (этиленгликоль, глицерин, ксилит).
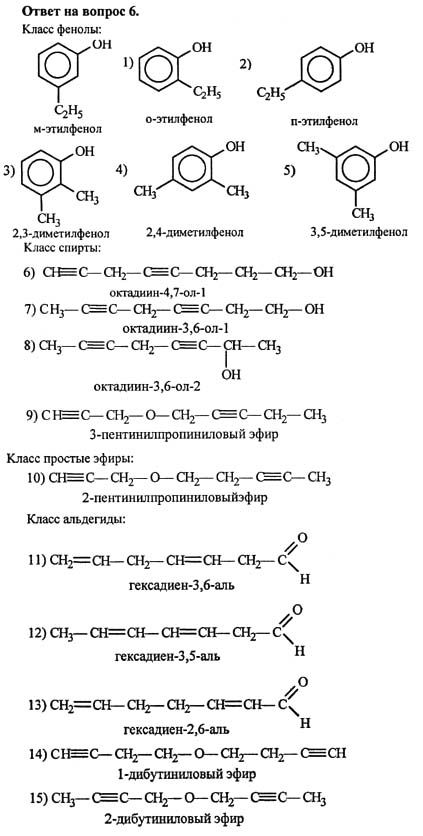
Фенолы. Строение и физические свойства фенола. Взаимное влияние атомов в молекуле фенола. Химические свойства фенола: реакции с натрием, щелочами, бромной водой. Применение фенолов.
Загрязнение окружающей среды фенолсодержащими отходами. Понятие о диоксине.
- Карбонильные соединения. Нуклеофильное присоединение
Альдегиды и кетоны. Карбонильная группа, ее особенности. Изомерия, номенклатура, физические свойства. Химические свойства альдегидов. Понятие о механизме реакций нуклеофильного присоединения. Окисление. Качественные реакции на альдегидную группу. Применение формальдегида, уксусного альдегида, ацетона. Фенолформальдегидные смолы.
- Карбоновые кислоты. Производные кислот. Поликонденсация.
Карбоновые кислоты. Строение карбоксильной группы. Номенклатура. Физические свойства, роль водородных связей. Одноосновные и многоосновные карбоновые кислоты. Химические свойства карбоновых кислот – взаимодействие с металлами, основными оксидами, основаниями, спиртами. Соли карбоновых кислот. Муравьиная, уксусная, щавелевая, пальмитиновая, стеариновая, лимонная и салициловая кислоты – особенности строения и свойств этих соединений, их применение.
Одноосновные и многоосновные карбоновые кислоты. Химические свойства карбоновых кислот – взаимодействие с металлами, основными оксидами, основаниями, спиртами. Соли карбоновых кислот. Муравьиная, уксусная, щавелевая, пальмитиновая, стеариновая, лимонная и салициловая кислоты – особенности строения и свойств этих соединений, их применение.
Понятие о производных карбоновых кислот – получение, свойства, применение.
Применение сложных эфиров. Понятие об эфирных маслах. Ацетилсалициловая кислота.
Жиры. Строение жиров, свойства и роль в организме. Гидрирование и гидролиз жиров в промышленности.
Мыла. Понятие о механизме моющего действия. Синтетические моющие средства
- Углеводы
Углеводы. Типы углеводов: моно-, ди- и полисахариды. Глюкоза, фруктоза, рибоза, дезоксирибоза: представление о пространственном строении, физические и химические свойства, нахождение в природе, роль в процессах жизнедеятельности. Качественные реакции на альдегидную и диольную группы. Открытая и циклическая формы моносахаридов. Гликозидный гидроксил.
Качественные реакции на альдегидную и диольную группы. Открытая и циклическая формы моносахаридов. Гликозидный гидроксил.
Олиго- и полисахариды. Представление о пространственном строении сахарозы. Восстанавливающие и невосстанавливающие сахариды. Целлюлоза, крахмал, гликоген. Общее и различие в строении и свойствах. Гидролиз целлюлозы и крахмала. Физиологическая роль полисахаридов. Применение крахмала и целлюлозы. Искусственные волокна, бумага.
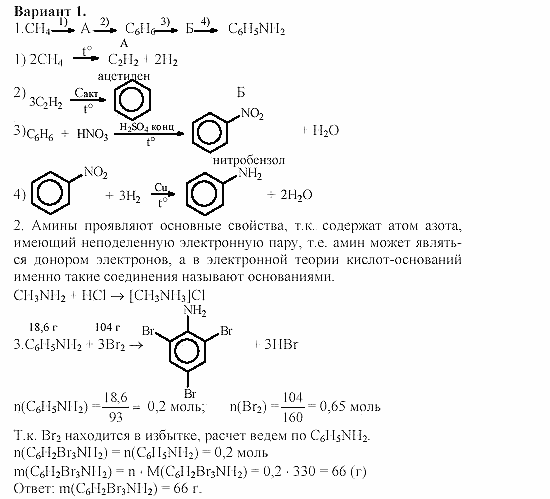
- Нитропроизводные. Амины
Нитросоединения. Электронное и пространственное строение нитрогруппы. Общая характеристика химических свойств. Реакция Зинина.
Амины. Типы аминов. Изомерия. Номенклатура, физические и химические свойства. Основность аминов. Реакции и применение анилина. Понятие о реакциях азосочетания и азокрасителях.
- Аминокислоты, белки, гетероциклы, нуклеиновые кислоты
Аминокислоты. Строение, названия, кислотно-основные свойства, амфотерность, пептидная связь. Роль аминокислот в процессах жизнедеятельности.
Роль аминокислот в процессах жизнедеятельности.
Белки. Ди- и полипептиды. Гидролиз. Понятие о первичной, вторичной, третичной и четвертичной структуре белков, их роль и функция в организме. Денатурация белков.
Понятие о гетероциклических соединениях. Пиридин и пиррол. Нуклеиновые кислоты – строение и функции в организме. Строение нуклеозидов и нуклеотидов. АТФ и АДФ.
Grade 10 — CIC Secondary School
Contact Information
Ms. Brigette Javier
Google Meet Code:
Grade 10- 1: sdsnmsz
Избранные ссылки
Академия Хана Химик y
0008
High School Chemistry
Syllabi
Q1 Syllabus
Q2 Syllabus
Q3 Syllabus
Q4 Syllabus
10th Grade Chemistry
Химия – это экспериментальная наука, сочетающая академическое изучение с приобретением практических и исследовательских навыков. Темы этого курса будут включать основы научных исследований и измерений, структуру вещества и атома, периодическую таблицу, химическую связь, химические реакции и стехиометрию, состояния вещества, термохимию и равновесие, ядерную химию и органическую химию. Студенты также сделают независимое исследовательское эссе по теме химии по своему выбору.
Темы этого курса будут включать основы научных исследований и измерений, структуру вещества и атома, периодическую таблицу, химическую связь, химические реакции и стехиометрию, состояния вещества, термохимию и равновесие, ядерную химию и органическую химию. Студенты также сделают независимое исследовательское эссе по теме химии по своему выбору.
Textbook: Modern Chemistry , Sarquis and Sarquis, Houghton Mifflin Harcourt, 2017
Upcoming Homework & Tests
Periodic Table, SI Unit Conversions, Polyatomic Ions, Activity Series
Chemistry Essay Схема
Рубрика сочинения по химии
Анализ ошибок
Как подготовиться и сдать тест
Test Strategies
How To Read Textbooks
S1 Exam Study Guide
Unit 1 Q1
Introduction to Chemistry
Unit 2 Q1
Атомы и электронные конфигурации
Блок 3 Q2
Периодический закон
1
Unit 4 Q2
Chemical Bonding and Reactions
Unit 5 Q3
Chemical Quantities
Unit 6 Q3
States
Блок 7 Q3
Термохимия и равновесие
Nuclear Chemistry
Unit 9 Q4
Organic Chemistry
Websites
Pre-Chemistry Prep or Post-Chemistry Review :
https://www. khanacademy.org/science/chemistry Пройдите любой из уроков, перечисленных на этом сайте.
khanacademy.org/science/chemistry Пройдите любой из уроков, перечисленных на этом сайте.
http://sciencespot.net/Pages/classchem.html Пройдите любой из интернет-уроков, чтобы попрактиковаться в изучении химии и словарном запасе.
https://www.onlinemathlearning.com/high-school-chemistry.html Выполните любой из уроков на этой странице (читайте, смотрите видео и решайте практические задачи).
Предфизическая подготовка:
https://www.khanacademy.org/science/physics Выполните любой из уроков с этой страницы.
http://www.physicsclassroom.com/ Прочтите учебники по физике, попробуйте интерактивные занятия по физике, а затем пройдите викторины на обзорной сессии.
http://sciencespot. net/Pages/classphys.html Посещайте любые интернет-уроки, чтобы попрактиковаться в физике и словарном запасе.
net/Pages/classphys.html Посещайте любые интернет-уроки, чтобы попрактиковаться в физике и словарном запасе.
10 класс Наука: химия карточки
Похожие карточки
Пожалуйста, войдите, чтобы добавить в папки.
Войти
Вы создали 2 папки. Пожалуйста, обновитесь до Cram Premium, чтобы создавать сотни папок!
Обновление
- Перемешивание
Включить
Выключить
- В алфавитном порядке
Включить
Выключить
- Передний Первый
Включить
Выключить
- Обе стороны
Включить
Выключить
- Читать
Включить
Выключить
Чтение. ..
..
Фронт
9029Диапазон из 4 карт для изучениячерез
Кнопка воспроизведения
Кнопка воспроизведения
Прогресс
1/18
Нажмите, чтобы перевернуть
Используйте клавиши со стрелками ВЛЕВО и ВПРАВО для перемещения между карточками;
Используйте клавиши со стрелками ВВЕРХ и ВНИЗ, чтобы перевернуть карту;
H показать подсказку;
A читает текст в речь;
- Делиться
- Распечатать
- Экспорт
- Клон
18 карт в этом наборе
- Передний
- Спина
Химическая номенклатура и создание химических формул: Ионные соединения | ||
Найдите в книге многоатомные ионы и соединения для изучения | ||
Word и сбалансированные скелетные уравнения | Пример: 2Na+Cl2= 2NaCl Посмотрите в учебнике по химии, чтобы изучить остальные | |
Типы химических реакций | 1. Пример: натрий + кислород = оксид натрия 2. Разложение Пример: оксид магния = магний + кислород 3. Одиночное смещение Пример: хлор + бромид калия = хлорид калия + бром 64 4. Двойное вытеснение Пример: хлорид бария + йодид калия = йодид бария + хлорид калия 5. Горение Пример: метан + кислород = медь + вода 6. Нейтрализация Пример: NaOH + HCl = NaCl + h3O | |
Сжигание углеводородов | Тип реакции, при которой углеводород реагирует с кислородом с образованием углекислого газа, воды и тепла. | |
Скорости химических реакций | 1. Температура Пример: повышение температуры приведет к увеличению скорости реакции из-за увеличения количества столкновений с высокой энергией. 2. Концентрация Пример: Если концентрация растворенного реагента увеличивается, частицы реагента становятся более скученными. 3. Площадь поверхности Пример: Если площадь поверхности реагента увеличить, то скорость реакции увеличится. 4. Катализаторы Пример: Катализаторы повышают скорость реакции, не будучи израсходованными, они делают это, приводя в действие необходимую энергию для активации. | |
Шкала PH, индикаторы и объяснение шкалы | Индикатор PH — это химическое вещество, которое в небольших количествах добавляется в раствор для визуального отображения степени слышимости или щелочности раствора путем изменения цвета в небольшом диапазоне значений PH. Шкала PH находится в диапазоне от 0 до 14 и используется для классификации водных растворов как кислых, щелочных или нейтральных. | |
Кислоты и основания и нейтрализация | Кислоты — это соединения, которые имеют шпористый вкус, при растворении в воде они выделяют ионы водорода. Основания — это соединения с горьким вкусом. Многие основания представляют собой ионные соединения, которые разделяются на ионы металлов и гидроксид-ионы. Нейтрализация: когда соединение не является ни кислотным, ни щелочным и имеет рН 7. | |
Периодическая таблица | ||
Химические и физические свойства веществ, включая металлы, неметаллы, металлоиды, галогены, благородные газы | Физические свойства: Металл: металлы сильно различаются по твердости, пластичности, пластичности, плотности и температуре плавления. Неметалл: большинство неметаллов хранится при комнатной температуре. Они могут быть очень хрупкими и плохо проводить электричество и тепло. Металлоиды: обычно твердые и имеют металлический блеск. Хрупкое электричество и имеет среднюю передачу тепла. Металлоиды: обычно твердые вещества с металлическим блеском. Хрупкое электричество и имеет среднюю передачу тепла. Галогены: имеют низкие температуры плавления и кипения и становятся темнее по мере уменьшения группы галогенов. Благородные газы: меньшего порядка и меньшего цвета, это газы с минимальным атомом углерода и очень низкой химической реакцией. Химические свойства: Металлы: металлы очень реакционноспособны, металл имеет тенденцию легко терять электроны и образовывать положительные ионы. Неметалл: имеет склонность делить электроны с другими атомами. Металлоиды: легко образуют газы и реагируют с галогенами, образуя соединения. Благородные газы: имеют очень низкую химическую активность. | |
Индикаторы химического и физического изменения | Физическое изменение: — изменение цвета — изменение температуры — образование осадков — образование газа Химическое изменение: — Появление пузырьков или газа — Странные формы — Изменение температуры плавления и кипения | |
Катализатор | Катализатор — это вещество, которое ускоряет химическую реакцию, но не расходуется в ходе химической реакции. | |
Ионные, ковалентные и молекулярные связи | Подробнее см. в книге. | |
Удельная теплоемкость | Теплота, необходимая для повышения температуры единицы массы данного вещества на заданную величину | |
Уровень Валентности | Уровни валентности — это уровни диаграммы Бора-Резерфорда. | |
атом или молекула с суммарным электрическим зарядом из-за потери или приобретения одного или нескольких электронов. | ||
Диаграммы Бора-Резерфорда для атомов | Подробнее см. |
